题目内容
【题目】下列离子方程式书写正确的是( )
A.NaHS的水解:HS-+ H2O![]() S2-+ H3O+
S2-+ H3O+
B.NaHCO3在水溶液中的电离:HCO3+ H2O![]() H2 CO3+ OH
H2 CO3+ OH
C.NH4Cl的水解:NH4+ + H2O = NH3·H2O + OH
D.硫酸铝溶液和碳酸氢钠溶液混合: Al3+ + 3HCO3 = Al(OH)3↓+3CO2↑
【答案】D
【解析】
A项、NaHS是强碱弱酸盐,HS—在溶液中水解使溶液呈碱性,水解的离子方程式为HS-+ H2O![]() H2S+ OH,故A错误;
H2S+ OH,故A错误;
B项、NaHCO3在水溶液中电离出碳酸根离子和氢氧根离子,电离方程式为HCO3+ H2O![]() CO32-+ H+,故B错误;
CO32-+ H+,故B错误;
C项、NH4Cl是强酸弱碱盐,铵根离子在溶液中水解导使溶液呈酸性,水解的离子方程式为NH4+ + H2O ![]() NH3·H2O + H+,故C错误;
NH3·H2O + H+,故C错误;
D项、硫酸铝是强酸弱碱盐,碳酸氢钠是强碱弱酸酸式盐,铝离子和碳酸氢根离子在溶液中发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为Al3+ + 3HCO3 = Al(OH)3↓+3CO2↑,故D正确;
故选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
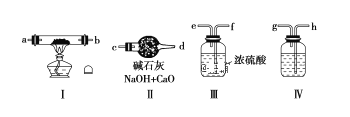
小学生10分钟应用题系列答案【题目】已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
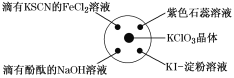
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变成蓝色 | Cl2具有氧化性 |
A.AB.BC.CD.D
【题目】阅读下面信息,推断元素,按要求回答问题:
信息 | 问题 |
①短周期元素X、Y、Z、W,原子序数依次增大,最外层电子数均不少于最内层电子数 | (1)X一定不是__ A.氢 B.碳 C.氧 D.硫 |
②一定条件下,上述四种元素的单质均能与足量的氧气反应,生成的氧化物有两种能溶于稀硫酸,三种能溶于浓NaOH溶液,氧化物的相对分子质量都大于26 | (2)这四种元素中有铝元素吗?__ |
③向上述四种元素的单质的混合物中,加入足量的盐酸,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中有白色沉淀 | (3)白色沉淀的化学式为__ |
④向上述四种元素的单质的混合物中,加入足量的烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸,最终溶液中有白色沉淀 | (4)生成白色沉淀的离子方程式为__ |
⑤X与W同主族 | (5)X的最高价氧化物的电子式为___ |