��Ŀ����
����Ŀ����֪M�Ƕ����ڽ���Ԫ�أ�X��Y�Ƕ����ڷǽ���Ԫ�أ���X��M��Y��ԭ��������������������ɵ�����M3XY(����ΪM2XMY)��һ�����õ����ӵ��塣�о����ڳ�ѹ���������з�Ӧ�ϳ�M3XY: 2M + 2MXA +2MY==2M3XY +A2�����г��³�ѹ��A2����ɫ��ζ���壬��֪������Ӧ������0.92 g M�ĵ��ʿɵõ���״����448 mL��A2�������й�˵����ȷ����
A.�����Ӱ뾶��Y��M��X
B.���⻯��ķе㣺XС��Y
C.MXA�ǹ��ۻ�����
D.M3XY����ˮ����Һ�ʼ���
���𰸡�D
��������
����2M+2MXA+2MY=2M3XY +A2���ɵù�ϵʽ2M ~ A2�� ����������ݣ���֪n(A2) =![]() =0.02mol������M��A2�����ʵ�����ϵ��n(M)=0.04mol��0.92 g M��Ħ����������
=0.02mol������M��A2�����ʵ�����ϵ��n(M)=0.04mol��0.92 g M��Ħ����������![]() ����M�ĵ��ʵ�Ħ������=23gmol-1����M�Ƕ����ڽ���Ԫ�أ���M��Na��M��Y���γɻ�����MY����ԭ������M��Y��Y���Ƕ����ڷǽ���Ԫ�أ���Y��Cl����M3XY(M2X.MY)��XԪ�صĻ��ϼ���-2�ۣ���ԭ������X��M������X��O�����³�ѹ��A2����ɫ��ζ���壬���������Ӧ��MXA��A�Ļ��ϼ�Ϊ+1����֪AΪH���ʹ˷������
����M�ĵ��ʵ�Ħ������=23gmol-1����M�Ƕ����ڽ���Ԫ�أ���M��Na��M��Y���γɻ�����MY����ԭ������M��Y��Y���Ƕ����ڷǽ���Ԫ�أ���Y��Cl����M3XY(M2X.MY)��XԪ�صĻ��ϼ���-2�ۣ���ԭ������X��M������X��O�����³�ѹ��A2����ɫ��ζ���壬���������Ӧ��MXA��A�Ļ��ϼ�Ϊ+1����֪AΪH���ʹ˷������
A�����Ӳ�����ͬʱ�����Ӳ���Խ�࣬�뾶Խ�����Ӳ�����ͬʱ���˵����Խ�뾶ԽС�����Ӱ뾶�Ĵ�С˳��Ϊr(C1-)��r(O2-)��r(Na+ )����A����
B��H2O����֮�����������е����HCl����B����
C��MXA��NaOH���Ǻ��й��ۼ������ӻ������C����
D��M3 XY(Na2O.NaCl)����ˮ���ˮ������Ӧ����NaOH��NaCl����Һ�Լ��ԣ���D��ȷ��
��ѡD��

����Ŀ�������������͵���Ҫ�ɷ�֮һ���������������Ҫ���壺
��ӦI�����ѽ⣩��CH3COOH(g)2CO(g)+2H2(g) ��H1
��ӦII�����Ȼ�����CH3COOH(g)CH4(g)+CO2(g) ��H2
��֪����ӦI�Ļ��Ϊ��E5-E2��kJ����ӦI�淴Ӧ�Ļ��Ϊ��E5-E3��kJ����ӦII�Ļ��Ϊ��E4-E2��kJ����ӦII�淴Ӧ�Ļ��Ϊ��E4-E1��kJ��E1��E5������������
��1����H1+��H2=___________kJ/mol (���й�E�Ĵ���ʽ��ʾ)��
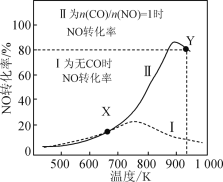
��2���ڲ�ͬ�¶��£����ܱ������г������������������Ӧ��ͬʱ���ø�����IJ������¶ȵĹ�ϵ��ͼ��ʾ��

��Լ650��֮ǰ���������ʵ��ڼ����ԭ���ǣ�________________________________��
��Լ650��֮�������¶����ߺ��������ʸ��ڼ����ԭ���ǣ�___________�������ţ�
a. ��ӦII���ʼ���
b. ��ӦI���ʼӿ�ij̶ȱȷ�ӦII��
c. ��ӦI�����ƶ�������ӦII�����ƶ�
d. ��ӦI�����ƶ��ij̶ȴ��ڷ�ӦII�����ƶ��ij̶�
������ͼ���������������һ������������ĸ���Ӧ�������ǣ�______________��
��3��Ͷ��һ���������ᣬ����ͬѹǿ�£�������ͬ��Ӧʱ��������ʵ�����ݣ�
�¶ȣ����� | ���� | CH3COOHת���� | H2��ѡ���� |
550 | �� | 14.5 | 40.2 |
550 | �� | 11.1 | 62.1 |
600 | �� | 11.2 | 41.2 |
600 | �� | 10.3 | 63.3 |
��H2��ѡ���ԣ�ת����CH3COOH������H2�İٷֱ���
������ʵ�����ݱ���������ͬ�¶��²�ͬ�Ĵ�����CH3COOHת����H2��ѡ������������Ӱ�죬��ԭ����________��
�����������CH3COOHת��ΪH2ƽ��ת���ʵĴ�ʩ��________��
A��ʹ�ô����� B��ʹ�ô�����
C�����߷�Ӧ�¶� D�����ӷ�Ӧ���Ũ��