题目内容
7.室温下,1mol无水硫酸铜(CuSO4)溶于水放出a kJ的热,胆矾(CuSO4•5H2O)受热失水的热化学方程式为CuSO4•5H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4(s)+5H2O(s)△H=+b kJ/mol,又知胆矾溶于水会使溶液温度降低,则a、b的关系为( )| A. | a<b | B. | a>b | C. | a=b | D. | 无法确定 |
分析 已知CuSO4•5H2O(s)=CuSO4(s)+5H2O(l);△H=+bKJ/mol;CuSO4(s)=Cu2+(aq)+SO42-(aq);△H=-akJ/mol;
胆矾溶于水时,溶液温度降低,反应为CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H′>0;根据盖斯定律确定△H′与a、b的关系
解答 解:已知①CuSO4•5H2O(s)=CuSO4(s)+5H2O(l);△H=+bKJ/mol;
②CuSO4(s)=Cu2+(aq)+SO42-(aq);△H=-akJ/mol;
③CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H′>0;
根据盖斯定律:方程③=方程①+方程②,
所以△H′=b+(-a)>0,即b>a,
故选A.
点评 本题考查了物质溶解恒容物质分解过程中的能量变化,根据盖斯定律分析物质溶解过程中的能量变化是解题关键,题目难度中等.

练习册系列答案
相关题目
15.取三张湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加98.3%的硫酸、新制氯水、浓氨水,三张试纸最后呈现的颜色是( )
| A. | 红、白、蓝 | B. | 黑、白、蓝 | C. | 白、白、蓝 | D. | 黑、红、蓝 |
12.下列有关蛋白质的说法中,不正确的( )
| A. | 鸡蛋清溶液滴入浓硝酸微热有黄色沉淀生成 | |
| B. | 采用多次盐析和溶解,可以分离提纯蛋白质 | |
| C. | 用稀释后的福尔马林浸泡种子会使蛋白质变性 | |
| D. | 蛋白质是仅由C、H、O三种元素组成的高分子化合物 |
19.下列化学用语表达正确的是( )
| A. | 苯的分子式 | B. | 氟原子的结构示意图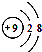 | ||
| C. | 氯化钠的电子式 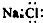 | D. | 正丁烷的结构简式CH3(CH2)2CH3 |
16.有机物数量繁多的主要原因是( )
| A. | 有机物中含有多种元素 | B. | 碳原子最外层有4个电子 | ||
| C. | 有机物的副反应多 | D. | 有机物存在同分异构现象 |
17.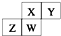 如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
 如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | z的最高正化合价与最低负化合价的绝对值可能相等 | |
| D. | w的最高价氧化物的水化物可能为弱酸,也有可能为强酸 |