题目内容
17.实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入碎瓷片,目的是防止暴沸.
(2)反应中加入过量的乙醇,目的是提高乙酸的转化率.
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏.这样操作可以提高酯的产率,其原因是及时加热蒸出乙酸乙酯,有利于平衡向生成酯的方向移动
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
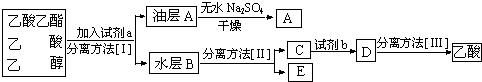
则试剂a是:饱和的碳酸钠溶液,分离方法I是分液,分离方法Ⅱ是蒸馏,
试剂b是:稀硫酸,分离方法Ⅲ是蒸馏.
分析 (1)对于液体加热蒸馏,应加入碎瓷片,防止暴沸;
(2)乙酸与乙醇的酯化反应是可逆反应,反应中通常加入过量的乙醇,提高乙酸的转化率;
(3)及时加热蒸出乙酸乙酯,有利于平衡向生成酯的方向移动;
(4)粗产品乙酸乙酯中含有乙酸与乙醇,用饱和的碳酸钠溶液反应掉乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,便于溶液分层,乙酸乙酯密度比水小,乙酸乙酯在上层,然后利用分液,乙酸乙酯加入无水碳酸钠吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸钠、乙酸钠,进行蒸馏可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再进行蒸馏可以收集乙酸.
解答 解:(1)对于液体加热蒸馏,应加入碎瓷片,防止暴沸;故答案为:碎瓷片,防止暴沸;
(2)乙酸与乙醇的酯化反应是可逆反应,反应中通常加入过量的乙醇,提高乙酸的转化率;故答案为:提高乙酸的转化率;
(3)及时加热蒸出乙酸乙酯,有利于平衡向生成酯的方向移动,可以提高酯的产率;故答案为:及时加热蒸出乙酸乙酯,有利于平衡向生成酯的方向移动;
(4)粗产品乙酸乙酯中含有乙酸与乙醇,用饱和的碳酸钠溶液反应掉乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,便于溶液分层,乙酸乙酯密度比水小,乙酸乙酯在上层,然后利用分液,乙酸乙酯加入无水碳酸钠吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸钠、乙酸钠,进行蒸馏可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再进行蒸馏可以收集乙酸;故答案为:饱和的碳酸钠溶液;分液;蒸馏;稀硫酸;蒸馏.
点评 本题考查乙酸乙酯的制备,难度不大,注意实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理,(4)中试剂b选择,由于盐酸易挥发,不能使用盐酸.

练习册系列答案
相关题目
6.100mL浓度为2mol•L-1的硫酸跟过量的锌片反应,某同学想加快反应速率,又不影响成氢气的总量,下列操作不符合要求的是( )
| A. | 将锌片换成等量的锌粉 | B. | 加入数滴氯化铜溶液 | ||
| C. | 升高温度 | D. | 加入适量的6mol•L-1的硫酸 |
5.在恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件达新平衡,其反应过程如图.下列说法中错误的是( )


| A. | 新旧平衡态时,A的体积分数相同 | |
| B. | 由旧平衡变为新平衡态,平衡常数不变 | |
| C. | 旧平衡态的v正与新平衡态的v逆相等 | |
| D. | t2时刻速率突变的原因是向密闭容器中加C或B |
12. 实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
(1)选择仪器.完成本实验所必需的仪器有:托盘天平(精确到0.1g)、药匙、烧杯、玻璃棒、500 mL 容量瓶、胶头滴管以及等质量的几片滤纸.
(2)计算.配制该溶液需取NaCl晶体的质量为14.6g.
(3)称量.
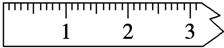
①天平调平之后,应将天平的游码调至某个位置,请在图中用一根竖线标出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的左盘(填“左盘”或“右盘”).
③称量完毕,将药品倒入烧杯中.
(4)溶解.该步实验中需要使用玻璃棒,目的是搅拌,加速溶解.
(5)转移、洗涤.在转移时应使用玻璃棒引流,洗涤烧杯2~3次是保证溶质全部转移至容量瓶中.
(6)定容,摇匀.
(7)在配制溶液(或者稀释浓溶液)的过程中,存在引起误差的一些错误操作,可能造成所配溶液的浓度会受到影响,请完成表格(在空格处填偏大、偏小或者无影响).
 实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.(1)选择仪器.完成本实验所必需的仪器有:托盘天平(精确到0.1g)、药匙、烧杯、玻璃棒、500 mL 容量瓶、胶头滴管以及等质量的几片滤纸.
(2)计算.配制该溶液需取NaCl晶体的质量为14.6g.
(3)称量.
①天平调平之后,应将天平的游码调至某个位置,请在图中用一根竖线标出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的左盘(填“左盘”或“右盘”).
③称量完毕,将药品倒入烧杯中.
(4)溶解.该步实验中需要使用玻璃棒,目的是搅拌,加速溶解.
(5)转移、洗涤.在转移时应使用玻璃棒引流,洗涤烧杯2~3次是保证溶质全部转移至容量瓶中.
(6)定容,摇匀.
(7)在配制溶液(或者稀释浓溶液)的过程中,存在引起误差的一些错误操作,可能造成所配溶液的浓度会受到影响,请完成表格(在空格处填偏大、偏小或者无影响).
| 引起误差的一些错误操作 | 对CB的影响 |
| 定容时,俯视刻度线 | 偏大 |
| 转移溶液时,玻璃棒下端靠在容量瓶刻度线以上 | 偏小 |
| 洗涤量取浓溶液的量筒并将洗涤液转移到容量瓶 | 偏大 |
| 定容后,经振荡、摇匀、静置、液面低于刻度线再加水 | 偏小 |
2.下列关于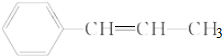 的说法正确的是( )
的说法正确的是( )
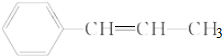 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子都可能在同一平面上 | |
| B. | 最多只可能有6个碳原子在同一平面上 | |
| C. | 有5个原子可能在同一直线上 | |
| D. | 所有原子可能在同一平面上 |
9.下列装置或操作能达到实验目的是( )
| A. | 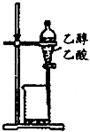 除去乙醇中的乙酸 | B. | 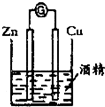 形成原电池 | ||
| C. |  制取乙酸乙酯 制取乙酸乙酯 | D. | 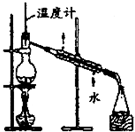 石油的分馏 |
6.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记录,“银针验毒”的原理是4Ag+2H2S+O2═2Ag2S+2H2O下列有关该反应的说法正确的是( )
| A. | Ag是氧化物 | B. | O2被氧化 | ||
| C. | H2S发生还原反应 | D. | H2S未发生电子转移 |
 、
、 .
.