题目内容
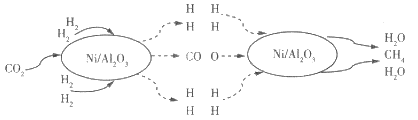
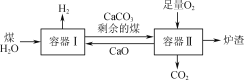
【题目】一种制氢技术原理如图所示。容器Ⅰ中发生的某反应a为C(s)+2H2O(g)![]() CO2(g)+2H2(g);ΔH。下列有关说法正确的是( )
CO2(g)+2H2(g);ΔH。下列有关说法正确的是( )
A.已知反应a在一定条件下能够自发进行,则该反应的ΔH<0
B.向容器Ⅰ中加入CaO能有效实现H2与CO2的分离
C.剩余的煤进入容器Ⅱ是为了充分利用其与O2反应放出的热量
D.煤中含有的S在容器Ⅱ中最终转化为CaSO3进入炉渣
【答案】BC
【解析】
煤和H2O一起进入容器I,发生反应:C(s)+2H2O(g)![]() CO2(g)+2H2(g),将H2抽出,剩下的CO2与容器II产生的CaO反应,生成CaCO3。再将CaCO3和剩余的煤一起投入容器II,在容器II中发生反应:CaCO3
CO2(g)+2H2(g),将H2抽出,剩下的CO2与容器II产生的CaO反应,生成CaCO3。再将CaCO3和剩余的煤一起投入容器II,在容器II中发生反应:CaCO3 ![]() CaO+ CO2↑;C+ O2
CaO+ CO2↑;C+ O2 ![]() CO2,生成的CaO可投入容器I循环使用。最终剩余的固体即为炉渣。
CO2,生成的CaO可投入容器I循环使用。最终剩余的固体即为炉渣。
A.△G=△H-T△S,若△G<0说明反应可自发进行。反应a为C(s)+2H2O(g)![]() CO2(g)+2H2(g),是气体体积增大的反应,即熵增反应(△S>0),因此若反应的△H>0,在温度比较高的条件下,也可以满足△G<0,A错误;
CO2(g)+2H2(g),是气体体积增大的反应,即熵增反应(△S>0),因此若反应的△H>0,在温度比较高的条件下,也可以满足△G<0,A错误;
B.向容器Ⅰ中加入CaO,发生反应CaO+ CO2= CaCO3,气体只剩H2,有效的实现H2与CO2的分离,B正确;
C.CaCO3的分解需要高温的条件,CaCO3 ![]() CaO+ CO2↑,C和O2的反应可以放热,为CaCO3的分解提供能量,C正确;
CaO+ CO2↑,C和O2的反应可以放热,为CaCO3的分解提供能量,C正确;
D.煤中含有的S在容器Ⅱ中最终转化为CaSO4,SO2+CaO=CaSO3,2CaSO3+O2=2CaSO4,D错误;
故选BC。

【题目】(1)在一固定容积的密闭容器中进行如下反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其平衡常数K和温度T的关系如下:
CO(g)+H2O(g),其平衡常数K和温度T的关系如下:
T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
①K的表达式为____________________;
②该反应的正反应为__________反应(“吸热”或“放热”);
③下列选项中,能判断该反应已经达到化学平衡状态的是____________(填字母代号)。
A.容器中压强不变 B.混合气体中CO浓度不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(2)下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl,溶液呈碱性的有__________(填序号);常温下0.01 mol/L HCl溶液的pH=________;pH=11的CH3COONa溶液中由水电离产生的c(OH-)=________。
(3)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
①若向该溶液中滴加NaOH溶液,则先沉淀的是 ____________(填离子符号);
②判断Ksp[Mg(OH)2]____________Ksp[Fe(OH)2](填“>”、“=”或“<”)。
(4)电解装置如图所示:
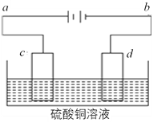
①当用惰性电极电解时,d电极的反应式为____________;
②若用此装置进行铁上镀铜,已知镀层金属采用纯铜且电镀前两电极材料质量相等,电镀一段时间后对电极进行称量发现两极质量差为16 g,则电路中转移的电子为____________mol。