题目内容
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是
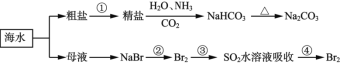
A.制取NaHCO3的反应是利用其溶解度小于NaCl
B.侯氏制碱应先通NH3再通CO2
C.在第②、③、④步骤中,溴元素均被氧化
D.③④的目的是进行溴的富集
【答案】C
【解析】
A. 往精盐溶液中通入氨气和二氧化碳,得到碳酸氢钠沉淀,说明碳酸氢钠的溶解度小于氯化钠,故A正确;
B. 由于CO2在水中的溶解度较小,而NH3的溶解度较大,所以要在食盐水先通NH3然后再通CO2,否则CO2通入后会从水中逸出,等再通NH3时溶液中CO2的量就很少了,这样得到的产品也很少,故B正确;
C. 在第②、④步骤中溴离子转化为溴单质,溴的化合价升高失电子,被氧化,步骤③中溴单质和二氧化硫反应生成硫酸和溴化氢,溴元素化合价降低得电子被还原,故C错误;
D. 浓缩后增大溴离子的浓度,与氯气发生2Br-+C12=Br2+2CI-,用空气和水蒸气将溴吹出,并用SO2氧化吸收,从而达到富集溴,③中发生Br2+ 2H2O+SO2=2HBr+H2SO4,④中发生Cl2+ 2HBr=Br2+ 2HCI,则③④的目的是进行溴的富集,故D正确;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
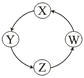
【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
Al | NaAlO2 | Al(OH)3 | Al2O3 | ||
② | Na | NaOH | Na2CO3 | NaCl | |
③ | C | CO | CO2 | H2CO3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①② B. ①③④ C. ②③ D. ①④