题目内容
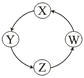
【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
Al | NaAlO2 | Al(OH)3 | Al2O3 | ||
② | Na | NaOH | Na2CO3 | NaCl | |
③ | C | CO | CO2 | H2CO3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①② B. ①③④ C. ②③ D. ①④
【答案】A
【解析】
①铝与氢氧化钠溶液反应生成偏铝酸钠,偏铝酸钠与足量的二氧化碳反应生成氢氧化铝,氢氧化铝受热分解为氧化铝,符合转化关系,故①正确;
②钠与水反应生成氢氧化钠,氢氧化钠与碳酸反应生成碳酸钠,碳酸钠与稀盐酸反应生成氯化钠,熔融氯化钠电解生成钠,故②正确;
③碳在氧气中不完全燃烧生成一氧化碳,一氧化碳与氧气继续反应生成二氧化碳,二氧化碳与水反应生成碳酸,碳酸加热分解为二氧化碳,不能生成碳,不符合转化关系,故③错误;
④铁与氯气反应可生成氯化铁,氯化铁溶液与铁反应可得到氯化亚铁溶液,氯化亚铁与氢氧化钠生成氢氧化亚铁,氢氧化亚铁加热分解得不到铁,不符合转化关系,故④错误;
故正确选项为①②。
综上所述,本题选A。

练习册系列答案
相关题目