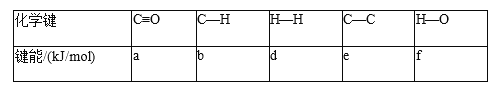
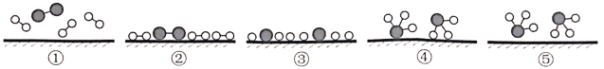
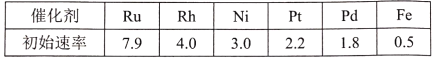
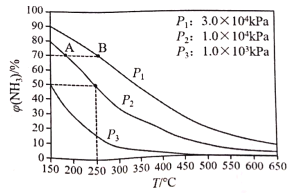
题目内容
【题目】如图有机物分子中带“![]() ”碳原子就是手性碳原子。该有机物分别发生下列反应,生成的有机物分子中仍含有手性碳原子的是
”碳原子就是手性碳原子。该有机物分别发生下列反应,生成的有机物分子中仍含有手性碳原子的是
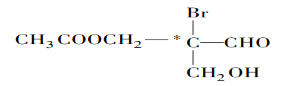
A.与乙酸发生酯化反应B.与NaOH水溶液反应
C.与银氨溶液作用只发生银镜反应D.催化剂作用下与![]() 反应
反应
【答案】C
【解析】
A.该有机物与乙酸发生酯化反应后,—CH2OH转化为—CH2OOCCH3,分子中含有相同的原子团—CH2OOCCH3,不再含有手性碳原子,故A错误;
B.该有机物与NaOH水溶液发生水解反应后,—Br原子转化为—OH、—CH2OOCCH3转化为—CH2OH,分子中含有相同的原子团—CH2OH,不再含有手性碳原子,故B错误;
C.该有机物与与银氨溶液作用发生银镜反应后,—CHO转化为-COONH4,分子中没有相同的原子团,还含有手性碳原子,故C正确;
D.该有机物在催化剂作用下与![]() 发生加成反应后,—CHO转化为转化为—CH2OH,分子中含有相同的原子团—CH2OH,不再含有手性碳原子,故D错误;
发生加成反应后,—CHO转化为转化为—CH2OH,分子中含有相同的原子团—CH2OH,不再含有手性碳原子,故D错误;
故选C。

【题目】二氧化氮可由NO和O2生成,已知在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g) ΔH, n(NO)、n(O2)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
n(O2)/mol | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(1)该反应的化学平衡常数表达式为K=___________________
(2)已知:K800 ℃>K1 000 ℃,则该反应的ΔH_________0(填“大于”或“小于”),
(3)用O2表示0~2 s内该反应的平均速率为_________。
(4)能说明该反应已达到平衡状态的是_________。
a.容器内气体颜色保持不变 b.2υ逆(NO)=υ正(O2)
c.容器内压强保持不变 d.容器内气体密度保持不变
(5)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动,应采取的措施有____。
A.升温 B.加入氧气 C. 降温 D.增大压强
(6)在800 ℃时,计算通入2 mol NO和1 mol O2的平衡常数K=_________
(7)已知下列反应在某温度下的平衡常数以及ΔH
H2(g)+S(s) H2S(g) K1 ΔH1
S(s)+O2(g) SO2(g) K2 ΔH2
则在该温度下反应H2(g)+SO2(g) O2(g)+H2S(g) K3 ΔH3
平衡常数K3=__________(用含有K1 K2的式子表示);
其反应热ΔH3=________(用含有ΔH1 ΔH2的式子表示)