题目内容
【题目】多晶硅是制作光伏电池的关键材料。将SiCl4氢化为SiHCl3的热化学方程式为:3SiCl4+2H2(g)+Si(s)![]() 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0
(1)该反应是____________反应(填吸热、放热)
(2)在相同条件,相同时间t时,不同温度下该反应中SiCl4转化率如图所示。下列叙述正确的是________________(填序号)。
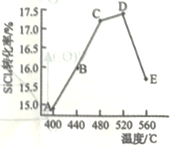
a.相同时间t内,A点的平均反应速率大于B点
b.相同时间t时,B点:v正>v逆
c.相同时间t时,v逆:C点大于A点
d.工业生产中采用了适宜温度:480~520°C
(3)为了增大化学反应速率,除加入催化剂、升高温度外还可以采用哪些方法和措施:___。(只写出一条)
【答案】放热 bcd 将固体Si粉碎增大接触面积、增大反应物浓度、加入反应物增大压强(只填增大压强不得分)
【解析】
(1) 已知△H2<0,则该反应为放热反应;
(2) a.相同时间t内,A点的温度小于B点,则A点的平均反应速率小于B点,与题意不符,a错误;
b.相同时间t时,B点未达到平衡状态,反应正向进行,则v正>v逆,符合题意,b正确;
c.相同时间t时,C点的温度大于A点,则v逆:C点大于A点,符合题意,c正确;
d.根据图像可知,温度在480~520°C时,SiCl4的转化率最高,则工业生产中采用了适宜温度:480~520°C,符合题意,d正确;
(3) 将固体Si粉碎增大接触面积、增大反应物浓度、加入反应物增大压强均可提高反应速率。
(1) 已知△H2<0,则该反应为放热反应;
(2) a.相同时间t内,A点的温度小于B点,则A点的平均反应速率小于B点,与题意不符,a错误;
b.相同时间t时,B点未达到平衡状态,反应正向进行,则v正>v逆,符合题意,b正确;
c.相同时间t时,C点的温度大于A点,则v逆:C点大于A点,符合题意,c正确;
d.根据图像可知,温度在480~520°C时,SiCl4的转化率最高,则工业生产中采用了适宜温度:480~520°C,符合题意,d正确;
答案为bcd;
(3) 将固体Si粉碎增大接触面积、增大反应物浓度、加入反应物增大压强均可提高反应速率。