��Ŀ����
����Ŀ�����Ȼ���������ýȾ����������ͼװ�ÿ����Ʊ����Ȼ��������ּг�װ������ȥ����

�й���Ϣ���±���
��ѧʽ |
|
|
Ħ�������� | 190 | 261 |
�۵� | 246 | -33 |
�е� | 652 | 144 |
�������� | ��ɫ���壬������ | ��ɫҺ�壬��ˮ�� |
�ش��������⣺
��1��װ�ü�������![]() ������Ϊ_____________��
������Ϊ_____________��
��2����װ�ü���ȡ������![]() ����ԭΪ
����ԭΪ![]() ���÷�Ӧ�����ӷ���ʽΪ___________��
���÷�Ӧ�����ӷ���ʽΪ___________��
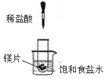
��3������ͼװ�����Ӻã��ȼ��װ�������ԣ�����������Ũ���ᣬ���۲쵽___________��������ʼ����װ�ö������ۻ����ʵ�����������������������װ�ö�����ʱ��������װ�ö���Ŀ���ǣ��ٴٽ�����������Ӧ����_________________________��
��4�����ȱ��װ���ң����ܷ����ĸ���Ӧ�Ļ�ѧ����ʽΪ_______________��װ�ü���������______������ĸ���ţ���
A.��ȥδ��Ӧ����������ֹ��Ⱦ����
B.��ֹ������![]() �������װ����
�������װ����
C.��ֹˮ��������װ������Թ���ʹ����ˮ��
D.��ֹ������![]() ����װ������Թ���ʹ��������
����װ������Թ���ʹ��������
��5��ijͬѧ��Ϊ��װ���еķ�Ӧ���ܲ���![]() ���ʣ������Լ��п����ڼ���Ƿ����
���ʣ������Լ��п����ڼ���Ƿ����![]() ����______������ĸ���ţ���
����______������ĸ���ţ���
A. ![]() ��Һ B.
��Һ B. ![]() ��Һ������
��Һ������![]() ��Һ�� C.
��Һ�� C. ![]() ��Һ
��Һ
��6����Ӧ����ȥ����![]() ����Ӧ������װ�õ��Թ����ռ���
����Ӧ������װ�õ��Թ����ռ���![]() ����
����![]() �IJ���Ϊ_____������3λ��Ч���֣���
�IJ���Ϊ_____������3λ��Ч���֣���
���𰸡�������ƿ ![]() ===
=== ![]() ��װ���ڳ�������ɫ���� ʹ
��װ���ڳ�������ɫ���� ʹ![]() ���������ڴӻ�����з������
���������ڴӻ�����з������ ![]() =
=![]() AC B 88.1%
AC B 88.1%
��������
��ʵ���Ŀ�����Ʊ����Ȼ����������Ʊ�������������Ϊ��ֹ������Ⱦ�����������巴Ӧ�������β���������������ᴿ��ò�Ʒ��Χ����һ˼·���������⡣
��1��װ�ü�������![]() Ϊ������ƿ��
Ϊ������ƿ��
��2�����������Ũ���ᷴӦ��ȡ����ʱ��![]() ����ԭΪ
����ԭΪ![]() ��Cl-������ΪCl2�����ӷ���ʽΪ
��Cl-������ΪCl2�����ӷ���ʽΪ![]() ===
=== ![]() ��
��
��3��Ϊ��װ�ö����Ƶ����Ȼ�����������װ�ü������ɵ��������벢����װ�ö���ʼ����װ�ö���Ϊ������Ȼ����IJ��ʣ����ٸ���Ʒ�Ȼ����������ɣ����ۻ����ʵ�����������������������װ�ö��������ٽ�����������Ӧ����ʹ![]() �����ӻ�����з��������
�����ӻ�����з��������
��4��װ�����еı���ʳ��ˮ�ɳ�ȥ�����е�HCl���ʣ���ȱ��װ���ң�װ�ö��з�������Ӧ![]() =
=![]() ��
��
![]() ������װ�����б�������Һ�壬δ��Ӧ��������װ�ü��еļ�ʯ�����գ�������Ⱦ�������ӱ�����Ϣ֪
������װ�����б�������Һ�壬δ��Ӧ��������װ�ü��еļ�ʯ�����գ�������Ⱦ�������ӱ�����Ϣ֪![]() ��ˮ�⣬���Ʊ����ռ�
��ˮ�⣬���Ʊ����ռ�![]() ��װ���ڲ�����ˮ���룬װ�ü�����һ�����Ƿ�ֹˮ��������װ������Թ���ʹ����ˮ�⣬ѡ��AC��
��װ���ڲ�����ˮ���룬װ�ü�����һ�����Ƿ�ֹˮ��������װ������Թ���ʹ����ˮ�⣬ѡ��AC��
��5��Ҫ����![]() ��Ʒ���Ƿ����
��Ʒ���Ƿ����![]() ���ʣ�Ӧ�����Ƿ����Sn2+���������仹ԭ�Լ��顣��Ʒ�м������
���ʣ�Ӧ�����Ƿ����Sn2+���������仹ԭ�Լ��顣��Ʒ�м������![]() ��
��![]() ��Һ������ɫ��ȥ����
��Һ������ɫ��ȥ����![]() ��B������
��B������![]() ��Һ������Sn2+��������������
��Һ������Sn2+��������������![]() ��Һ��
��Һ��![]() ��
��![]() ����Ӧ�����ɰ�ɫ������A��C����������
����Ӧ�����ɰ�ɫ������A��C����������
��6��n(Sn)=1.19g/119g��mol-1=0.01mol�����۲���n(SnCl4)=0.01mol��ʵ�ʲ���n(SnCl4)=2.3g/261g��mol-1=0.00881mol��![]() �IJ���=(0.00881mol/0.01mol)��100%=88.1%��
�IJ���=(0.00881mol/0.01mol)��100%=88.1%��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ������װ���ܴﵽʵ��Ŀ�ĵ���
ѡ�� | A | B | C | D |
ʵ��װ�� |
|
|
|
|
ʵ��Ŀ�� | ̽��Na2CO3��NaHCO3�ܽ�ȵ���Դ�С | ����֪Ũ�ȵ�NaOH��Һ�ζ�δ֪Ũ�ȵ�ϡ���� | ����������Ũ���ᷴӦ������CO2 | ��֤þ��ϡ����ķ�Ӧ����ЧӦ |
A. A B. B C. C D. D