题目内容
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,该溶液放在用惰性电极材料做电极的电解槽中,通电片刻,则氧化产物与还原产物质质量比为…( )
| A.35.5:108 | B.16:207 | C.8:1 | D.108:35.5 |
C
解析试题分析:在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,首先发生反应:Ag++Cl-="AgCl↓;" Pb2++SO42-= PbSO4↓;因此得到的溶液为NaNO3溶液。阳离子的放电顺序是H+> Na+;阴离子的放电顺序是: OH->含氧酸根离子。该电解反应实质是电解水。因此通电片刻,氧化产物O2与还原产物H2的物质的量的比为1 :2,质量比为32:4=8:1。因此选项为C。
考点:考查离子反应、电解的应用的知识。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是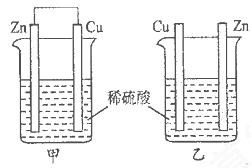
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的酸性均减弱 | D.产生气泡的速率甲比乙慢 |
固体电解质是通过离子迁移传递电荷。如RbAg4I5晶体,其中迁移的物种全是Ag+,利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图。被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是( )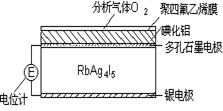
| A.Ag-e-=Ag+ | B.I2+2Ag++2e-=2AgI |
| C.I2+2Rb++2e-=2RbI | D.4AlI3+3O2=2Al2O3+6I2 |
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法正确的是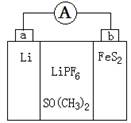
| A.该装置将电能转化为化学能 |
| B.Li+向a极移动 |
| C.可以用水代替SO(CH3)2做溶剂 |
| D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
下列有关原电池的说法中,正确的是( )
| A.铝片和镁片用导线连接后插入NaOH溶液中,镁片较活泼,作负极 |
| B.铝片和铜片用导线连接后插入浓硝酸中,铜作负极 |
| C.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| D.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用锌片作负极,铁片作正极,FeCl3溶液作电解质 |
用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是( ) 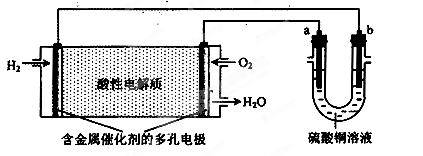
| A.a为负极,b为正极 |
| B.若a极是铁,b极是铜,b极逐渐溶解,a极上有铜析出 |
| C.若a、b极都是石墨,在相同条件下,理论上a极产生的气体与电池中消耗的O2体积相等 |
| D.若电解精炼粗铜时,b极是粗铜,a极是纯铜 |
下列描述中,不符合生产实际的是 ( )
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 | B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | D.在镀件上电镀锌,用锌作阳极 |
汽车的启动电源常用铅蓄电池。其结构如下图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O根据此反应判断下列叙述中正确的是
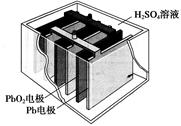
| A.PbO2是电池的负极 |
| B.放电时,溶液中的H+向正极区移动,正极区域的溶液的酸性增强 |
| C.放电时,电子由Pb电极通过导线流向PbO2 |
| D.正极的电极反应式为Pb-2e-=Pb2+ |
某原电池总反应为2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3 |
| B.正极为C,负极为Fe,电解质溶液为Fe(NO)3 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3 |
| D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3 |