题目内容
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法正确的是
| A.该装置将电能转化为化学能 |
| B.Li+向a极移动 |
| C.可以用水代替SO(CH3)2做溶剂 |
| D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
D
解析试题分析:A、该装置是原电池,化学能转化为电能,A不正确;B、锂是活泼的金属,因此负极是锂,即a是负极,发生反应为:Li-e-═Li+。原电池中阳离子向正极移动,则Li+向b极移动,B不正确;C、锂是活泼的金属,极易与水反应,则不能用水代替SO(CH3)2做溶剂,C不正确;D、根据总反应式以及负极反应式可知,b极反应式是FeS2+4Li++4e-=Fe+2Li2S,故D正确,故选D。
考点:考查电化学原理的应用

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是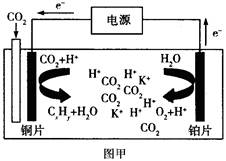
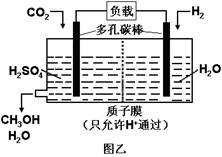
| A.甲中铜片作阴极,K+向铜片电极移动 |
| B.乙中正极发生的电极反应为CO2+6e-+6H+=CH3OH+H2O |
| C.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
| D.乙中H2SO4的作用是增强溶液的导电性 |
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,该溶液放在用惰性电极材料做电极的电解槽中,通电片刻,则氧化产物与还原产物质质量比为…( )
| A.35.5:108 | B.16:207 | C.8:1 | D.108:35.5 |
某锂电池的电池总反应为4Li+2SOCl2=4LiCl+S+SO2,下列有关说法正确的是( )
| A.锂电极作电池负极,放电过程中发生还原反应 |
| B.1 mol SOCl2发生电极反应转移的电子数为4 mol |
| C.电池的正极反应为2SOCl2+2e-=4Cl-+S+SO2 |
| D.组装该电池必须在无水、无氧的条件下进行 |
下列关于原电池的叙述中错误的是
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.原电池是将化学能转变为电能的装置 |
| C.在原电池中,电子流出的一极是负极,发生氧化反应 |
| D.原电池放电时,电流的方向是从正极经导线到负极 |
一种碳纳米管(氢气)二次电池原理如右下图。该电池的电解质为6mol/L KOH溶液,下列说法正确的是
| A.储存H2的碳纳米管放电时为负极,充电时为阳极 |
| B.充电时阳极反应为NiO(OH)+H2O+e﹣=Ni(OH)2+OH﹣ |
| C.放电时正极附近溶液的pH减小 |
| D.放电时负极反应为H2+2OH﹣﹣2e﹣=2H2O |