题目内容
固体电解质是通过离子迁移传递电荷。如RbAg4I5晶体,其中迁移的物种全是Ag+,利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图。被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是( )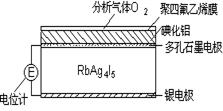
| A.Ag-e-=Ag+ | B.I2+2Ag++2e-=2AgI |
| C.I2+2Rb++2e-=2RbI | D.4AlI3+3O2=2Al2O3+6I2 |
C
解析试题分析:由图可知,传感器中发生4AlI3+3O2=2Al2O3+6I2,原电池的负极发生Ag-e-=Ag+,正极发生I2+2Ag++2e-=2AgI,所以肯定没有的反应是I2+2Rb++2e-=2RbI,答案选C。
考点:考查原电池及氧化还原反应

练习册系列答案
相关题目
以石墨为电极,电解KI溶液(其中含有少量酚酞和淀粉)。下列说法错误的是
| A.阴极附远溶液呈红色 | B.阴极逸出气体 |
| C.阳极附近溶液呈蓝色 | D.溶液的pH变小 |
全钒流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置, 其原理如图所示,其中H+的作用是参与正极反应,并通过交换膜定向移动使右槽溶液保持电中性。下列有关说法不正确的是( )
| A.放电时当左槽溶液逐渐由黄变蓝,其电极反应式为:VO2+ +e一+2H+=VO2+ +H2O |
| B.充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为l.0mol |
| C.充电时,H+由左槽定向移动到右槽 |
| D.充电过程中,右槽溶液颜色逐渐由绿色变为紫色 |
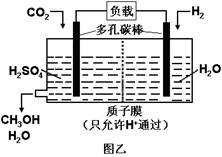
下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是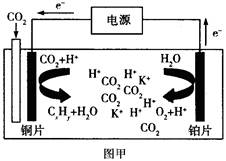
| A.甲中铜片作阴极,K+向铜片电极移动 |
| B.乙中正极发生的电极反应为CO2+6e-+6H+=CH3OH+H2O |
| C.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
| D.乙中H2SO4的作用是增强溶液的导电性 |
用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是( )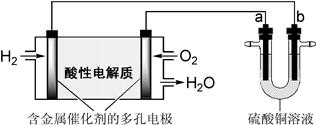
| A.燃料电池工作时,正极反应为:O2+ 2H2O + 4e- ="==" 4OH- |
| B.若a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.若a、b极都是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,该溶液放在用惰性电极材料做电极的电解槽中,通电片刻,则氧化产物与还原产物质质量比为…( )
| A.35.5:108 | B.16:207 | C.8:1 | D.108:35.5 |
某原电池总反应离子方程式为2Fe3++Fe===3Fe2+,能实现该反应的原电池是( )
| A.正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液 |
| B.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液 |
下列有关电池的叙述正确的是 ( )
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池工作时氢气在负极被氧化 |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
| D.氢氧燃料电池可将热能直接转变为电能 |
 2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH-⑥该电池的电解质溶液可能是碱液。其中正确的是
2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH-⑥该电池的电解质溶液可能是碱液。其中正确的是