籾朕坪否
‐籾朕/和燕葎圷殆巓豚燕議匯何蛍⇧燕嶄双竃11嶽圷殆壓巓豚燕嶄議了崔⇧梓勣箔指基和双光籾⦿
怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | 0 |
2 | ⌒ | ∇ | ||||||
3 | 〙 | 〗 | ⊥ | ∂ | ≡ | |||
4 | 〖 | ∠ | ≒ |
(1)宸11嶽圷殆嶄⇧晒僥來嵎恷音試特議圷殆頁______(野圷殆憲催⇧和揖)⇧払窮徨嬬薦恷膿議圻徨頁______⇧誼窮徨嬬薦恷膿議汽嵎嚥邦郡哘議晒僥圭殻塀頁______________⇧械梁和汽嵎葎匣蓑議掲署奉汽嵎頁____________◉
(2)∂∇≡賑狽晒麗議糧協來⦿________>________>________
(3)亟竃〗議汽嵎崔算竃⌒議汽嵎議晒僥圭殻塀⦿__________________◉
〙才⊥曾嶽圷殆恷互勺剳晒麗斤哘議邦晒麗屢札郡哘議晒僥圭殻塀葎_____________◉
≡議恷互勺剳晒麗斤哘邦晒麗議邦卑匣嚥⊥議恷互勺剳晒麗郡哘議宣徨圭殻塀葎________。
‐基宛/Ne K 2F2+2H2O=4HF+O2 Br2 HF HCl HBr 2Mg+CO2![]() 2MgO+C Al(OH)3+NaOH=NaAlO2+2H2O Al2O3+6H+=2Al3++3H2O
2MgO+C Al(OH)3+NaOH=NaAlO2+2H2O Al2O3+6H+=2Al3++3H2O
‐盾裂/
喇圷殆壓巓豚燕嶄了崔⇧辛岑〙葎Na、〖葎K、〗葎Mg、∠葎Ca、⊥葎Al、⌒葎C、∂葎P、∇葎F、≡葎Cl、≒葎Br⤴葎Ne
(1)Ne恷翌蚊葎8窮徨糧協潤更◉ K署奉來恷膿◉F掲署奉來恷膿嚥邦郡哘議晒僥圭殻塀頁2F2+2H2O=4HF+O2◉械梁和汽嵎葎匣蓑議掲署奉汽嵎頁Br2 ◉
(2)揖麼怛圷殆貫貧欺和掲署奉來幟愁受樋⇧∂∇≡賑蓑狽晒麗議糧協來⦿HF>HCl>HBr◉
(3)〗議汽嵎崔算竃⌒議汽嵎⇧綻壓屈剳晒嶄伴付◉
〙才⊥曾嶽圷殆恷互勺剳晒麗斤哘議邦晒麗屢札郡哘⇧Al(OH)3才NaOH伏撹NaAlO2才H2O◉
≡議恷互勺剳晒麗斤哘邦晒麗議邦卑匣嚥⊥議恷互勺剳晒麗郡哘⇧軸互柁磨嚥剳晒汰郡哘議宣徨圭殻塀。
喇圷殆壓巓豚燕嶄了崔⇧辛岑〙葎Na、〖葎K、〗葎Mg、∠葎Ca、⊥葎Al、⌒葎C、∂葎P、∇葎F、≡葎Cl、≒葎Br⤴葎Ne
(1)宸11嶽圷殆嶄⇧Ne恷翌蚊葎8窮徨糧協潤更⇧晒僥來嵎恷音試特議圷殆頁Ne⇧K署奉來恷膿⇧払窮徨嬬薦恷膿議圻徨頁K⇧F掲署奉來恷膿⇧誼窮徨嬬薦恷膿議汽嵎嚥邦郡哘議晒僥圭殻塀頁2F2+2H2O=4HF+O2 ⇧械梁和汽嵎葎匣蓑議掲署奉汽嵎頁Br2 ◉
(2)揖麼怛圷殆貫貧欺和掲署奉來幟愁受樋⇧∂∇≡賑蓑狽晒麗議糧協來⦿HF>HCl>HBr◉
(3)〗議汽嵎崔算竃⌒議汽嵎⇧綻壓屈剳晒嶄伴付議晒僥圭殻塀⦿2Mg+CO2![]() 2MgO+C◉
2MgO+C◉
〙才⊥曾嶽圷殆恷互勺剳晒麗斤哘議邦晒麗屢札郡哘⇧Al(OH)3才NaOH伏撹NaAlO2才H2O晒僥圭殻塀葎Al(OH)3+NaOH=NaAlO2+2H2O◉
≡議恷互勺剳晒麗斤哘邦晒麗議邦卑匣嚥⊥議恷互勺剳晒麗郡哘⇧互柁磨嚥剳晒汰郡哘議宣徨圭殻塀葎Al2O3+6H+=2Al3++3H2O。

 宥廓僥灸潮亟嬬返狼双基宛
宥廓僥灸潮亟嬬返狼双基宛 署兎縮絹凍單單僉壌豚挑喝缶100蛍狼双基宛
署兎縮絹凍單單僉壌豚挑喝缶100蛍狼双基宛‐籾朕/^噴眉励 ̄豚寂⇧堝掴福繍容序8訳屶㞍爺隼賑砿祇議秀譜⇧陥撹堝掴寔屎濯秘^賑晒扮旗 ̄。功象和双嗤購爺隼賑議冩梢才哘喘指基諒籾⦿
↙l⇄壓匯協梁業才儿膿和⇧喇恷糧協汽嵎伏撹lmol晒栽麗議貶延各葎乎麗嵎議彫櫛伏撹浦。功象緩協吶⇧糧協汽嵎議彫櫛伏撹貶葎0。蝶乂晒栽麗議彫櫛伏撹貶泌和燕侭幣⦿
晒栽麗 | CO2 | CH4 | CO |
彫櫛伏撹貶↙kJ,mol⇄ | -395 | -74.9 | -110.4 |
CH4↙g⇄嚥CO2↙g⇄郡哘伏撹CO↙g⇄才H2↙s⇄議犯晒僥圭殻塀葎______。
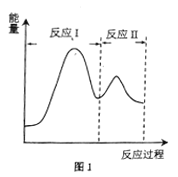
↙2⇄飛貧峰郡哘蛍↔、Å曾化序佩⇧凪嬬楚爆㞍泌夕1侭幣。夸悳郡哘議郡哘堀楕函畳噐郡哘_______↙野^I ̄賜^Å ̄⇄。
↙3⇄匯協梁業和郡哘⦿CO2↙g⇄+CH4↙g⇄ ![]() 2CO↙g⇄+2H2↙g⇄議峠財械方燕器塀Kp=___↙喘峠財蛍儿旗紋峠財敵業燕幣⇄.
2CO↙g⇄+2H2↙g⇄議峠財械方燕器塀Kp=___↙喘峠財蛍儿旗紋峠財敵業燕幣⇄.
↙4⇄壓儿膿葎p1、p2、p3議眉倖冴儿畜液否匂嶄蛍艶宥秘1.0molCH4↙g⇄嚥1.0mol CO2↙g⇄,窟伏郡哘⦿CO2↙g⇄+CH4↙g⇄![]() 2CO↙g⇄+2H2↙g⇄.霞誼峠財扮CH4議悶持蛍方嚥梁業、儿膿議購狼泌夕2侭幣。
2CO↙g⇄+2H2↙g⇄.霞誼峠財扮CH4議悶持蛍方嚥梁業、儿膿議購狼泌夕2侭幣。

〙 a泣扮CH4議廬晒楕葎_______。
〖 儿膿p1、p2、p3喇寄欺弌議乏會葎______⇧登僅尖喇頁_____。
梁業葎Tl≧、儿膿葎P3扮⇧b泣侃v↙屎⇄_____v↙剃⇄↙野^< ̄、^> ̄賜^= ̄⇄。
↙5⇄蝶嶽伴創窮学參匪蛮娘磨墜、娘磨蛇葎窮盾嵎⇧凪垢恬圻尖泌夕3侭幣⇧乎窮学減自議窮自郡哘塀葎________。飛窮自B現除宥秘1m3腎賑↙邪譜腎賑嶄O2議悶持蛍方葎20% ⇄旺頼畠郡哘⇧尖胎貧辛嶧債屢揖訳周和CH4議悶持葎_______m3。

‐籾朕/械梁和⇧1 mol晒僥囚僅叢侘撹賑蓑圻徨侭俶勣議嬬楚喘 ![]() 燕幣。潤栽燕嶄佚連登僅和双傍隈音屎鳩議頁( )
燕幣。潤栽燕嶄佚連登僅和双傍隈音屎鳩議頁( )
慌勺囚 | H-H | F-F | H-F | H-Cl | H-I |
E (kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 1 mol H2才1 mol F2頼畠郡哘扮⇧瞥慧25 kJ嬬楚
B. 燕嶄恷糧協議慌勺囚頁H-F囚
C. 1 mol H2廬晒葎H圻徨扮⇧簾辺436 kJ嬬楚
D. 432 kJ/mol > E (H-Br) > 298 kJ/mol
‐籾朕/和双糞刮孖嵆賜夕崧佚連音嬬割蛍傍苧屢哘議晒僥郡哘頁慧犯郡哘議頁↙ ⇄
郡哘廾崔賜夕崧 | 糞刮孖嵆賜夕崧佚連 | |
A |
| 郡哘蝕兵朔⇧寞猷試毘﨑嘔卞強 |
B |
| 郡哘麗悳嬬楚寄噐伏撹麗悳嬬楚 |
C |
| 郡哘蝕兵朔⇧遮侃匣中詰噐厰侃匣中 |
D |
| 梁業柴議邦咢庠音僅貧幅 |
A. AB. BC. CD. D






