题目内容
【题目】“十三五”期间,云南省将推进8条支线天然气管道的建设,促成云南真正迈入“气化时代”。根据下列有关天然气的研究和应用回答问题:
(l)在一定温度和压强下,由最稳定单质生成lmol化合物的焓变称为该物质的摩尔生成焙。根据此定义,稳定单质的摩尔生成焓为0。某些化合物的摩尔生成焓如下表所示:
化合物 | CO2 | CH4 | CO |
摩尔生成焓(kJ·mol) | -395 | -74.9 | -110.4 |
CH4(g)与CO2(g)反应生成CO(g)和H2(s)的热化学方程式为______。
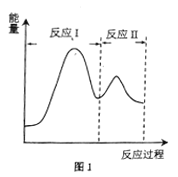
(2)若上述反应分Ⅰ、Ⅱ两步进行,其能量曲线如图1所示。则总反应的反应速率取决于反应_______(填“I”或“Ⅱ”)。
(3)一定温度下反应:CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)的平衡常数表达式Kp=___(用平衡分压代替平衡浓度表示).
2CO(g)+2H2(g)的平衡常数表达式Kp=___(用平衡分压代替平衡浓度表示).
(4)在压强为p1、p2、p3的三个恒压密闭容器中分别通入1.0molCH4(g)与1.0mol CO2(g),发生反应:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图2所示。
2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图2所示。

① a点时CH4的转化率为_______。
② 压强p1、p2、p3由大到小的顺序为______,判断理由是_____。
温度为Tl℃、压强为P3时,b点处v(正)_____v(逆)(填“<”、“>”或“=”)。
(5)某种燃料电池以熔融碳酸钠、碳酸钾为电解质,其工作原理如图3所示,该电池负极的电极反应式为________。若电极B附近通入1m3空气(假设空气中O2的体积分数为20% )并完全反应,理论上可消耗相同条件下CH4的体积为_______m3。

【答案】 CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) ΔH=+249.1kJ/mol I
2CO(g)+2H2(g) ΔH=+249.1kJ/mol I ![]() 80% p3>p2>p1 该反应为气体分子数增大的反应,压强增大,平衡逆移,甲烷的体积分数增大 > CH4+4CO32--8e-=5CO2+2H2O 0.1
80% p3>p2>p1 该反应为气体分子数增大的反应,压强增大,平衡逆移,甲烷的体积分数增大 > CH4+4CO32--8e-=5CO2+2H2O 0.1
【解析】(l)已知CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) 反应的ΔH=[2(-110.4)+0]kJ·mol-[(-395)+(-74.9)]kJ·mol=+249.1kJ/mol ,即CH4(g)与CO2(g)反应生成CO(g)和H2(s)的热化学方程式为CH4(g)+CO2(g)
2CO(g)+2H2(g) 反应的ΔH=[2(-110.4)+0]kJ·mol-[(-395)+(-74.9)]kJ·mol=+249.1kJ/mol ,即CH4(g)与CO2(g)反应生成CO(g)和H2(s)的热化学方程式为CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) ΔH=+249.1kJ/mol;
2CO(g)+2H2(g) ΔH=+249.1kJ/mol;
(2)根据能量曲线图可知,反应Ⅰ反应物活化能大,反应速率慢,而反应Ⅱ反应速率较快,则总反应的反应速率取决于慢反应,即反应I;
(3)可逆反应CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)的平衡常数表达式Kp=
2CO(g)+2H2(g)的平衡常数表达式Kp=![]() ;
;
(4)①设a点时CH4的转化率为α
CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
起始物质的量(mol) 1 1 0 0
变化物质的量(mol) α α 2α 2α
变化后物质的量(mol) 1-α 1-α 2α 2α
则: ![]() =
=![]() ,解得:α=80%;
,解得:α=80%;
② 该反应为气体分子数增大的反应,压强增大,平衡逆移,甲烷的体积分数增大,故p3>p2>p1;温度为Tl℃、压强为P3时,b点处恒压曲线P3上方,CH4的含量比平衡时高,则此时反应应正向进行,即v(正)>v(逆;
(5)燃料电池通O2的极为正极,通CH4的极为负极,即电极A为负极,负极上CH4失电子发生氧化反应,生成CO2,电极反应式为CH4+4CO32--8e-=5CO2+2H2O;若电极B附近通入1m3空气(假设空气中O2的体积分数为20% ),则参加反应的O2的物质的量为1000L×20%÷22.4L/mol,根据电子守恒可知,消耗CH4体积为1000L×20%÷22.4L/mol×![]() ×22.4L/mol=100L=0.1m3。
×22.4L/mol=100L=0.1m3。