题目内容
5.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故.根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会褪去.下列说法正确的是( )| A. | 处理过程中银器一直保持恒重 | |
| B. | 食盐溶液作为电解质溶液形成原电池 | |
| C. | 银器为正极,Ag2S被还原生成单质银 | |
| D. | 黑色褪去的原因是黑色Ag2S转化为白色AgCl |
分析 铝、银和电解质溶液构成原电池,铝作负极,银作正极,负极上铝失电子发生氧化反应,正极上银离子得电子发生还原反应,据此分析解答.
解答 解:A.银器放在铝制容器中,由于铝的活泼性大于银,故铝为负极,失电子,银为正极,银表面的Ag2S得电子,析出单质银,所以银器质量减小,故A错误;
B.铝、银和电解质溶液构成原电池,故B正确;
C.银作正极,正极上Ag2S得电子作氧化剂,在反应中被还原生成单质银,故C正确;
D.黑色褪去是Ag2S转化为Ag而不是AgCl,故D错误;
故选BC.
点评 本题考查原电池原理,明确正负极上得失电子是解本题关键,题目难度中等,注意盐的水解知识的应用.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
2.化学在可持续发展模式中正发挥着积极的作用.下列做法与可持续发展宗旨相违背的是( )
| A. | 推广碳捕集和存储技术,逐步实现二氧化碳零排放 | |
| B. | 对工业废水、生活污水净化处理,减少污染物的排放 | |
| C. | 加大铅蓄电池、含汞锌锰干电池的生产,满足消费需求 | |
| D. | 加大清洁能源的开发利用,提高资源的利用率 |
3.下列实验操作不能达到实验目的是( )
①用氢氧化钠溶液除去乙酸乙酯中混有的乙酸等杂质
②用分液漏斗分离乙醇和乙酸乙酯
③用乙醇和3%的硫酸共热到170℃制乙烯
④用加入浓溴水的方法分离苯和苯酚的混合物.
①用氢氧化钠溶液除去乙酸乙酯中混有的乙酸等杂质
②用分液漏斗分离乙醇和乙酸乙酯
③用乙醇和3%的硫酸共热到170℃制乙烯
④用加入浓溴水的方法分离苯和苯酚的混合物.
| A. | ①②③④ | B. | ①②③ | C. | ②③ | D. | ①④ |
20.研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如图1:
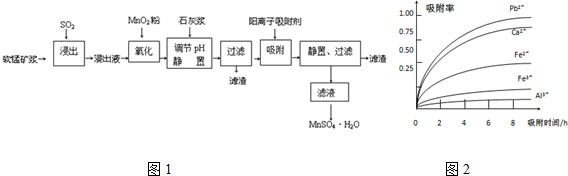
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
(1)浸出过程中生成Mn2+反应的化学方程式为SO2+MnO2=MnSO4,
(2)Fe2+被氧化的过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等(写二点).
(5)吸附步骤除去的主要离子为Pb2+、Ca2+.
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
(2)Fe2+被氧化的过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等(写二点).
(5)吸附步骤除去的主要离子为Pb2+、Ca2+.
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.
10.胡椒酚是植物挥发油中的一种成分,结构简式如图,关于胡椒酚的下列说法正确的是( )


| A. | 该化合物属于芳香烃 | |
| B. | 该化合物的分子式是 C9H11O | |
| C. | 分子中所有碳原子一定处于同一平面 | |
| D. | 1 mol该化合物最多可与4 mol H2发生反应 |
17.在下列各种石油的加工处理过程中,属于催化裂化过程的是( )
| A. | 分离汽油和煤油 | B. | 将重油分离为润滑油等 | ||
| C. | 将直链烃变为芳香烃 | D. | 十六烷变为辛烷和辛烯 |
14.下列物质用化学用语不正确的是( )
| A. | 乙烯的结构式:C2H4 | B. | HCl的电子式: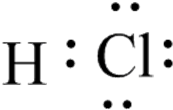 | ||
| C. | S2-的结构示意图: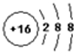 | D. | CO2的结构式:O=C=O. |
15.与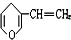 互为同分异构体的酚类化合物的同分异构体最多有( )
互为同分异构体的酚类化合物的同分异构体最多有( )
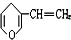 互为同分异构体的酚类化合物的同分异构体最多有( )
互为同分异构体的酚类化合物的同分异构体最多有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |