题目内容
15.与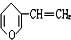 互为同分异构体的酚类化合物的同分异构体最多有( )
互为同分异构体的酚类化合物的同分异构体最多有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 同分异构体的酚类化合物,说明是含有苯环结构和酚羟基的同分异构体,根据结构可知该有机物不饱和度为4,只含有1个苯环,苯环的不饱和度为4,所以侧链不存在不饱和键,只有酚羟基和甲基,根据位置关系确定种类.
解答 解: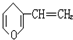 分子式为C7H8O,则该有机物不饱和度为4,含有1个苯环,苯环的不饱和度为4,则侧链不存在不饱和键,故侧链只有酚羟基和甲基,
分子式为C7H8O,则该有机物不饱和度为4,含有1个苯环,苯环的不饱和度为4,则侧链不存在不饱和键,故侧链只有酚羟基和甲基,
所以该有机物的同分异构体的酚类化合物有: 、
、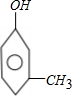 、
、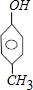 共3种,
共3种,
故选A.
点评 本题主要考查限制条件同分异构体的书写,题目难度中等,同分异构体主要有三种:碳链异构、官能团位置异构、官能团类别异构,明确书写原则为解答关键.

练习册系列答案
相关题目
5.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故.根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会褪去.下列说法正确的是( )
| A. | 处理过程中银器一直保持恒重 | |
| B. | 食盐溶液作为电解质溶液形成原电池 | |
| C. | 银器为正极,Ag2S被还原生成单质银 | |
| D. | 黑色褪去的原因是黑色Ag2S转化为白色AgCl |
6.正确掌握化学基本概念和化学用语是学好化学的基础,下列有关表述中正确的是( )
| A. | 过氧化氢与过氧化钠中含有化学键的类型完全相同 | |
| B. | NaHSO4在水溶液中的电离方程式为:NaHSO4═Na++H++SO42- | |
| C. | 因为NH4HCO3是强电解质,所以在其水溶液中只存在水解平衡,不存在电离平衡 | |
| D. | H216O、D216O、H218O、D218O互为同素异形体 |
3.现有乙酸和两种烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是( )
| A. | $\frac{1-a}{7}$ | B. | $\frac{3}{4}$a | C. | $\frac{6}{7}$(1-a) | D. | $\frac{12}{13}$(1-a) |
10.分子式为C6H12O2的酯经水解后,生成醇A和羧酸B,若A经氧化后生成B,则这种酯的结构可能有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
20.下列说法中,正确的是( )
| A. | 强电解质溶液一定比弱电解质溶液的导电性强 | |
| B. | 强电解质的水溶液中不存在分子 | |
| C. | 进行中和滴定时,锥形瓶不能用所盛溶液润洗 | |
| D. | 不同的弱电解质只要物质的量浓度相同,电离程度也相同 |
7.将0.2mol•L-1HCN溶液和0.1mol•L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是( )
| A. | c (HCN)<c (CN-) | B. | c (Na+)=c (CN-) | ||
| C. | c (HCN)-c (CN-)=c (OH-) | D. | c (HCN)+c (CN-)=0.1mol•L-1 |
4.下列关于淀粉和纤维素的叙述,正确的是( )
| A. | 分子式相同 | B. | 属于同一类物质 | C. | 互为同分异构体 | D. | 化学性质相同 |
5.下列有机物发生的反应属于加成反应的是( )
| A. | 乙烯使KMnO4溶液褪色 | B. | 乙烯使溴水褪色 | ||
| C. | 甲烷和氯气混合,见光 | D. | 用乙醇、乙酸与浓H2SO4 混合加热 |