题目内容
【题目】合金应用广泛,镍铜是重要的合金元素,如镧镍合金、铜镍合金、铝镍合金等。
![]() 基态铜原子的外围电子排布式为______,K和Cu属于同一周期,金属K的熔点比金属Cu______
基态铜原子的外围电子排布式为______,K和Cu属于同一周期,金属K的熔点比金属Cu______![]() 填“高”或“低”
填“高”或“低”![]() ,原因是______。
,原因是______。
![]() 在
在![]() 溶液中滴加稀氨水能形成配位化合物
溶液中滴加稀氨水能形成配位化合物![]() 。
。
![]() 、N、O、Ni的电负性由小到大的顺序为______;
、N、O、Ni的电负性由小到大的顺序为______;
![]() SO42-中S原子的杂化类型是______。
SO42-中S原子的杂化类型是______。
![]() SO42-与互为等电子体的分子的化学式
SO42-与互为等电子体的分子的化学式![]() 写出一种即可
写出一种即可![]() ______;
______;
![]() 工业上,采用反应
工业上,采用反应![]() 提纯粗镍。推测
提纯粗镍。推测![]() 晶体中存在的作用力有______。
晶体中存在的作用力有______。
![]() 非极性键
非极性键![]() 极性键
极性键![]() 范德华力
范德华力![]() 离子键
离子键![]() 配位键
配位键
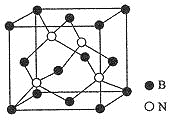
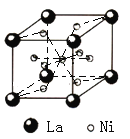
![]() 镧镍合金的晶胞如图1所示,镍原子除了1个在体心外,其余都在面上。该合金中镧原子和镍原子的个数比为______。
镧镍合金的晶胞如图1所示,镍原子除了1个在体心外,其余都在面上。该合金中镧原子和镍原子的个数比为______。
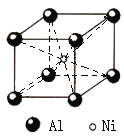
![]() 铝镍合金的晶胞如图所示。已知:铝镍合金的密度为
铝镍合金的晶胞如图所示。已知:铝镍合金的密度为![]() ,
,![]() 代表阿伏加德罗常数的数值,则镍、铝的最短核间距
代表阿伏加德罗常数的数值,则镍、铝的最短核间距![]() 为______。
为______。
【答案】![]() 低 K的原子半径大,价电子数少,金属键较弱
低 K的原子半径大,价电子数少,金属键较弱 ![]()
![]() 杂化
杂化 ![]() bce 1:5
bce 1:5 ![]()
【解析】
![]() 是29号元素,处于第四周期IB族,属于过渡元素,外围电子包括最外层电子与3d电子;原子半径越大、价电子越少,金属键越弱,金属晶体的熔点越低;
是29号元素,处于第四周期IB族,属于过渡元素,外围电子包括最外层电子与3d电子;原子半径越大、价电子越少,金属键越弱,金属晶体的熔点越低;
![]() 非金属性元素电负性大于金属元素的,同周期主族元素随原子序数增大电负性增大,N、O在它们的氢化物中均表现负化合价,它们的电负性均大于氢元素的;
非金属性元素电负性大于金属元素的,同周期主族元素随原子序数增大电负性增大,N、O在它们的氢化物中均表现负化合价,它们的电负性均大于氢元素的;
![]() 中S原子孤电子对数
中S原子孤电子对数![]() ,杂化轨道数目
,杂化轨道数目![]() ;
;
![]() 中含有5个原子、32个价电子,平均价电子数目为
中含有5个原子、32个价电子,平均价电子数目为![]() ,其等电子体的分子只能是价电子为7个4个原子与价电子为4个1个原子形成的分子;
,其等电子体的分子只能是价电子为7个4个原子与价电子为4个1个原子形成的分子;
![]() 晶体沸点很低,属于分子晶体,分子之间存在范德华力,
晶体沸点很低,属于分子晶体,分子之间存在范德华力,![]() 晶体中Ni与CO形成配位键,CO中原子之间形成极性键;
晶体中Ni与CO形成配位键,CO中原子之间形成极性键;
![]() 镍原子除了1个在体心外,其余都在面上,La处于晶胞顶点,均摊法计算晶胞中原子数目,确定原子数目之比;
镍原子除了1个在体心外,其余都在面上,La处于晶胞顶点,均摊法计算晶胞中原子数目,确定原子数目之比;
![]() 处于体对角线上的Al、Ni原子之间距离最近,二者距离等于晶胞体对角线长度的
处于体对角线上的Al、Ni原子之间距离最近,二者距离等于晶胞体对角线长度的![]() ,体对角线长度等于晶胞棱长的
,体对角线长度等于晶胞棱长的![]() 倍,均摊法计算晶胞中原子数目,计算晶胞质量,结合密度计算晶胞体积,晶胞体积开三次方得到晶胞棱长。
倍,均摊法计算晶胞中原子数目,计算晶胞质量,结合密度计算晶胞体积,晶胞体积开三次方得到晶胞棱长。
![]() 是29号元素,处于第四周期IB族,外围电子排布式为:
是29号元素,处于第四周期IB族,外围电子排布式为:![]() ,K的原子半径大,价电子数少,金属键较弱,故金属K的熔点比金属Cu的低,故答案为:
,K的原子半径大,价电子数少,金属键较弱,故金属K的熔点比金属Cu的低,故答案为:![]() ;低;K的原子半径大,价电子数少,金属键较弱;
;低;K的原子半径大,价电子数少,金属键较弱;
![]()
![]() 非金属性元素电负性大于金属元素的,同周期主族元素随原子序数增大电负性增大,N、O在它们的氢化物中均表现负化合价,它们的电负性均大于氢元素的,故电负性:
非金属性元素电负性大于金属元素的,同周期主族元素随原子序数增大电负性增大,N、O在它们的氢化物中均表现负化合价,它们的电负性均大于氢元素的,故电负性:![]() ,故答案为:
,故答案为:![]() ;
;
![]()
![]() 中S原子孤电子对数
中S原子孤电子对数![]() ,杂化轨道数目
,杂化轨道数目![]() ,S原子杂化方式为:
,S原子杂化方式为:![]() 杂化,故答案为:
杂化,故答案为:![]() 杂化;
杂化;
![]()
![]() 中含有5个原子、32个价电子,平均价电子数目为
中含有5个原子、32个价电子,平均价电子数目为![]() ,其等电子体的分子只能是价电子为7个4个原子与价电子为4个1个原子形成的分子,可能的等电子体分子式为:
,其等电子体的分子只能是价电子为7个4个原子与价电子为4个1个原子形成的分子,可能的等电子体分子式为:![]() 等,故答案为:
等,故答案为:![]() ;
;
![]()
![]() 晶体沸点很低,属于分子晶体,分子之间存在范德华力,
晶体沸点很低,属于分子晶体,分子之间存在范德华力,![]() 晶体中Ni与CO形成配位键,CO中原子之间形成极性键,没有非金属性与离子键,故答案为:bce;
晶体中Ni与CO形成配位键,CO中原子之间形成极性键,没有非金属性与离子键,故答案为:bce;
![]() 镍原子除了1个在体心外,其余都在面上,晶胞中Ni原子数目
镍原子除了1个在体心外,其余都在面上,晶胞中Ni原子数目![]() ,La处于晶胞顶点,晶胞中La原子数目
,La处于晶胞顶点,晶胞中La原子数目![]() ,该合金中镧原子和镍原子的个数比为1:5,故答案为:1:5;
,该合金中镧原子和镍原子的个数比为1:5,故答案为:1:5;
![]() 处于体对角线上的Al、Ni原子之间距离最近,二者距离等于晶胞体对角线长度的
处于体对角线上的Al、Ni原子之间距离最近,二者距离等于晶胞体对角线长度的![]() ,体对角线长度等于晶胞棱长的
,体对角线长度等于晶胞棱长的![]() 倍,晶胞中Al原子数目
倍,晶胞中Al原子数目![]() 、Ni原子数目
、Ni原子数目![]() ,故晶胞质量
,故晶胞质量![]() ,晶胞体积
,晶胞体积![]() ,晶胞棱长
,晶胞棱长![]() ,故镍、铝的最短核间距
,故镍、铝的最短核间距![]() ,
,
故答案为:![]() 。
。