题目内容
4.下列在指定溶液中的各组离子,一定能够大量共存的是( )| A. | 无色溶液中:CO32-、Al3+、Cl-、NO3- | |
| B. | 无色溶液中:NH4+、K+、CH3COO-、Cl- | |
| C. | pH=1的溶液中:Fe2+、NH4+、Mg2+、NO3- | |
| D. | 水电离的c(H+)=10-12 mol/L的溶液中:Fe3+、SO42-、K+、Na+ |
分析 A.碳酸根离子与铝离子发生双水解反应;
B.四种离子之间不反应,都是无色离子;
C.pH=1的溶液为酸性溶液,硝酸根离子在酸性条件下能够以后亚铁离子;
D.水电离的c(H+)=10-12 mol/L的溶液中存在大量氢离子或氢氧根离子,铁离子与氢氧根离子反应.
解答 解:A.CO32-、Al3+之间发生双水解反应,在溶液中不能大量共存,故A错误;
B.NH4+、K+、CH3COO-、Cl-之间不发生反应,且都是无色离子,在溶液中能够大量共存,故B正确;
C.pH=1的溶液中存在大量氢离子,Fe2+、NO3-发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.水电离的c(H+)=10-12 mol/L的溶液为酸性或碱性溶液,Fe3+与氢氧根离子反应,在碱性溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
15.下列说法正确的是( )
| A. | 镀锌铁皮的镀层损坏后,铁更容易腐蚀 | |
| B. | 镀锡铁皮的镀层损坏后,铁更容易腐蚀 | |
| C. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| D. | 钢铁吸氧腐蚀时,负极反应式为:2H2O+O2+4e-═4OH- |
12.下列根据实验现象所得出的结论中,一定正确的是( )
| A. | 无色试液加入Na2CO3溶液产生白色沉淀,结论:试液中含Ca2+ | |
| B. | 无色试液加入KOH溶液,加热产生的气体使湿润红色石蕊试纸变蓝,结论:试液中含NH4Cl | |
| C. | 无色试液使红色石蕊试纸变蓝,结论:试液呈碱性 | |
| D. | 无色试液焰色反应呈紫色,结论:试液是钾盐溶液 |
9.I.对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系.如表为几种弱酸在25℃时的电离平衡常数
回答下列问题:
(1)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是H2PO4-,最弱的是HPO42-.
(2)等浓度的下列溶液中由水电离出的OH-浓度由大到小的顺序是⑤③④①②(用序号作答)
①CH3COONa ②NaH2PO4 ③NaHPO4 ④NaHCO3 ⑤Na2CO3
(3)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的CH3COOH的电离转化率为?,则该温度下醋酸的电离平衡常数KCH3COOH$\frac{c{a}^{2}}{1-a}$.
II.已知t℃时,Kw=1×10-13;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=9:2.
III.现有含FeCl2杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按如图所示步骤进行提纯: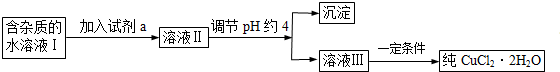
25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见如表:
请回答下列问题:
(1)流程中加入的试剂a最合适的是C(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是将Fe2+氧化为Fe3+,再除去.
(2)调节pH约4应该加入的物质可以是AC.
A.CuO B.CuCl2 C.Cu(OH)2 D.NaOH
利用平衡移动原理简述加入该物质的理由溶液中存在平衡Fe3++3H2O?Fe(OH)3+3H+,加入CuO或Cu(OH)2后,消耗溶液中H+,使平衡正向移动,从而使Fe3+转化为Fe(OH)3.
(3)最后能不能直接蒸发结晶得到CuCl2•2H2O?不能(填“能”或“不能”).如不能,应如何操作?(若能,此空不填)应在氯化氢气氛中浓缩后冷却结晶.
| 酸 | 电离平衡常数K |
| CH3COOH | 1.76×10-5 |
| H2CO3 | K1=4.31×10-7 K2=5.61×10-11 |
| H3PO4 | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
(1)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是H2PO4-,最弱的是HPO42-.
(2)等浓度的下列溶液中由水电离出的OH-浓度由大到小的顺序是⑤③④①②(用序号作答)
①CH3COONa ②NaH2PO4 ③NaHPO4 ④NaHCO3 ⑤Na2CO3
(3)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的CH3COOH的电离转化率为?,则该温度下醋酸的电离平衡常数KCH3COOH$\frac{c{a}^{2}}{1-a}$.
II.已知t℃时,Kw=1×10-13;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=9:2.
III.现有含FeCl2杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按如图所示步骤进行提纯:

25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见如表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 4.7 |
| 完成沉淀pH | 3.2 | 9.7 | 6.7 |
(1)流程中加入的试剂a最合适的是C(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是将Fe2+氧化为Fe3+,再除去.
(2)调节pH约4应该加入的物质可以是AC.
A.CuO B.CuCl2 C.Cu(OH)2 D.NaOH
利用平衡移动原理简述加入该物质的理由溶液中存在平衡Fe3++3H2O?Fe(OH)3+3H+,加入CuO或Cu(OH)2后,消耗溶液中H+,使平衡正向移动,从而使Fe3+转化为Fe(OH)3.
(3)最后能不能直接蒸发结晶得到CuCl2•2H2O?不能(填“能”或“不能”).如不能,应如何操作?(若能,此空不填)应在氯化氢气氛中浓缩后冷却结晶.
16.可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
| A. | 分别加入碘水,观察颜色反应 | B. | 分别加热,观察是否生成沉淀 | ||
| C. | 加入淀粉酶观察是否水解 | D. | 分别加入KI溶液,观察颜色反应 |
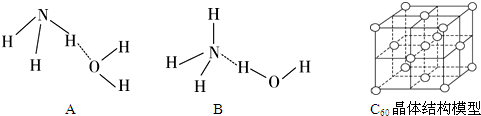
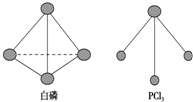 白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10.
白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10.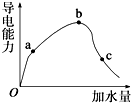 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: