题目内容
10.已知A,B,C,D四种短周期元素的原子序数依次增大,B的核电荷数是A、D核电荷数之和的$\frac{2}{3}$倍,A能分别与B、C、D形成电子总数相等的分子X、Y、Z.请回答下列问题:(1)A、C两元素的名称分别是:A氢,C氮
(2)B元素在周期表中的位置是第二周期、ⅣA族,D元素原子的结构示意图为
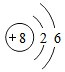 .
.(3)化合物BD2的电子式为
 ,Y的结构式为
,Y的结构式为 .
.(4)Y与C的最高正价氧化物的水化物刚好完全反应时,其生成物的化学式为NH4NO3,所含的化学键类型是离子.(填“离子”或“共价”化合物)
(5)用X、D2、NaOH溶液和铂(Pt)电极,可设计出一种燃料电池,则该燃料电池负极反应为CH4+10OH--8e-=CO32-+7H2O,正极反应为O2+H2O+4e-=4OH-.
分析 A、B、C、D四种短周期元素的原子序数依次增大,B的核电荷数是A、D核电荷数之和的$\frac{2}{3}$倍,结合原子序数可知,B处于第二周期,且处于偶数族,A能分别与B、C、D形成电子总数相等的分子X、Y、Z,考虑为氢化物,X为H元素,可推知B为C元素、C为N元素,D为O元素,X、Y、Z分别为CH4、NH3、H2O,以此解答该题.
解答 解:A、B、C、D四种短周期元素的原子序数依次增大,B的核电荷数是A、D核电荷数之和的$\frac{2}{3}$倍,结合原子序数可知,B处于第二周期,且处于偶数族,A能分别与B、C、D形成电子总数相等的分子X、Y、Z,考虑为氢化物,X为H元素,可推知B为C元素、C为N元素,D为O元素,X、Y、Z分别为CH4、NH3、H2O,
(1)由以上分析可知A为氢元素,C为氮元素,故答案为:氢;氮;
(2)B为C元素,位于周期表第二周期、ⅣA族,D为O元素,原子核外有2个电子层,最外层电子数为6,原子结构示意图为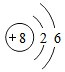 ,
,
故答案为:第二周期、ⅣA族;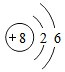 ;
;
(3)化合物CO2的电子式为 ,Y为NH3,结构式为
,Y为NH3,结构式为 ,故答案为:
,故答案为: ;
; ;
;
(4)Y与C的最高正价氧化物的水化物分别为NH3、HNO3,而刚好完全反应时,其生成物的化学式为NH4NO3,为离子化合物,
故答案为:NH4NO3;离子;
(5)甲烷燃料电池中,负极上投放燃料甲烷的电极是负极,负极上失电子发生氧化反应,电极反应式为:CH4+10OH--8e-=CO32-+7H2O,正极反应为O2+H2O+4e-=4OH-,
故答案为:CH4+10OH--8e-=CO32-+7H2O;O2+H2O+4e-=4OH-.
点评 本题考查结构性质位置关系、原电池等,题目比较综合,推断元素是解题关键,本题难点是元素的推断,需要学生熟练掌握基础知识,难度中等.

 名校课堂系列答案
名校课堂系列答案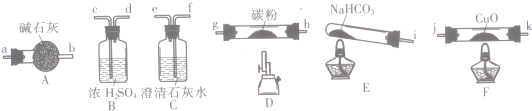
请回答:
(1)按气流方向,各装置从左到右的连接顺序为:i→cd→gh或hg→ab→jk或kj→fe尾气处理(填仪器接口的字母编号).
(2)说明CO能还原CuO的实验现象为F处硬质玻璃管中的黑色固体变为红色,C处澄清石灰水变浑浊.
(3)该实验处理尾气的方法为点燃烧掉或用气囊收集.
(4)若去掉B装置,可能产生的影响为NaHCO3分解产生的水蒸气高温能与碳粉反应生成H2,对实验产生干扰.
(5)将各装置按正确的顺序连接后进行实验.当反应结束后,F处硬质玻璃管中的固体全部变为红色.
[查阅资料]Cu和Cu2O均为红色;Cu2O在酸性溶液中能生成Cu和Cu2+.
[提出猜想]红色固体的成分可能为:①Cu;②Cu2O;③Cu和Cu2O.
[实验验证]该小组为验证上述猜想,分别取少量红色固体放人试管中,进行如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量稀硝酸、振荡 | 试管内红色固体完全溶解,溶液变为蓝色,并有无色气体产生 |
| b | 加入足量稀硫酸、振荡 | 试管内有红色固体,溶液为无色 |
[实验结论]根据上述实验结果,可知红色固体的成分为Cu(填化学式).
| A. | 棉、麻、羊毛、丝绸等天然衣着材料越来越受人们欢迎,它们的主要成分均为纤维素 | |
| B. | 晶体硅常用作太阳能电池板,它的工作原理符合电池原理 | |
| C. | 高炉炼铁、水泥工业、玻璃工业、海水制镁工业中都需要用到原料碳酸钙 | |
| D. | 雾霾中的PM2.5表面积大,分散在空气中形成胶体,吸附大量有毒有害物质,对人体造成严重危害 |
| A. | Na | B. | Cl2 | C. | H2 | D. | NaOH |
| A. | 臭氧层破坏--氟氯烃 | B. | 光化学烟雾--氮氧化物 | ||
| C. | 水体富营养化--含磷洗衣粉 | D. | 酸雨--二氧化碳 |
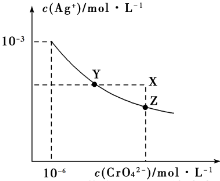
| A. | 在t℃时,Ag2CrO4的Ksp为1×10-12 | |
| B. | 在t℃时,AgCl的溶解度大于Ag2CrO4 | |
| C. | 在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点到X点 | |
| D. | 在t℃时,用AgNO3标准溶液滴定20mL未知浓度的KCl溶液,不能采用K2CrO4溶液为指示剂 |
 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验.请回答:
某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验.请回答: