题目内容
6.已知t℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,t℃时,在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )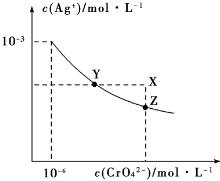
| A. | 在t℃时,Ag2CrO4的Ksp为1×10-12 | |
| B. | 在t℃时,AgCl的溶解度大于Ag2CrO4 | |
| C. | 在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点到X点 | |
| D. | 在t℃时,用AgNO3标准溶液滴定20mL未知浓度的KCl溶液,不能采用K2CrO4溶液为指示剂 |
分析 A、依据 图象曲线上的数据结合溶度积常数概念计算得到;曲线上的点是沉淀溶解平衡,溶度积是饱和溶液中离子浓度幂次方的乘积;
B、已知t℃时AgCl的Ksp=2×10-10,由A 知Ag2CrO4的Ksp为1×10-12,则c(AgCl)=$\sqrt{Ksp}$=$\sqrt{2×1{0}^{-10}}$=1.41×10-5,而c(Ag2CrO4)=$\root{3}{\frac{Ksp}{4}}$=$\frac{\root{3}{2}}{2}$×10-4;
C、在饱和Ag2CrO4溶液中加入K2CrO4仍为饱和溶液,点仍在曲线上;
D、用AgNO3溶液滴定过程中,AgCl先沉淀出来,待AgCl定量沉淀后,过量的一滴AgNO3溶液即与K2CrO4反应,形成Ag2CrO4砖红色沉淀.
解答 解:A、依据 图象曲线上的数据结合溶度积常数概念计算得到;曲线上的点是沉淀溶解平衡,Ag2CrO4的沉淀溶剂平衡为:Ag2CrO4(s)?2Ag+CrO42-,
Ksp=c2(Ag+)c(CrO42-)=(10-3)2×10-6=10-12,故A正确;
B、已知t℃时AgCl的Ksp=2×10-10,由A 知Ag2CrO4的Ksp为1×10-12,则c(AgCl)=$\sqrt{Ksp}$=$\sqrt{2×1{0}^{-10}}$=1.41×10-5,而c(Ag2CrO4)=$\root{3}{\frac{Ksp}{4}}$=$\frac{\root{3}{2}}{2}$×10-4,所以在t℃时,AgCl的溶解度小于Ag2CrO4,故B错误;
C、在饱和Ag2CrO4溶液中加入K2CrO4仍为饱和溶液,点仍在曲线上,所以在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点,故C错误;
D、用AgNO3溶液滴定过程中,由于AgCl的溶解度小,AgCl先沉淀出来,待AgCl定量沉淀后,过量的一滴AgNO3溶液即与K2CrO4反应,形成Ag2CrO4砖红色沉淀,则有砖红色沉淀生成时即达到终点,所以能采用K2CrO4溶液为指示剂,故D错误;
故选A.
点评 本题考查了沉淀溶解平衡的分析判断、溶度积常数的计算应用等,侧重于考查学生的分析能力和计算能力,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 钠和镁分别与冷水反应,判断钠和镁的金属性强弱 | |
| B. | 铁投入CuSO4溶液中置换出铜,判断铜与铁的金属性强弱 | |
| C. | 酸性H2CO3<HCl,判断氯与碳的非金属性强 | |
| D. | F2与Cl2分别与足量的H2反应的难易,判断氟与氯的非金属性强弱 |
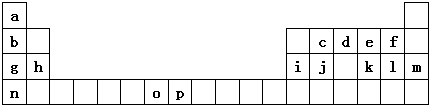
试回答下列问题:
(1)元素p的原子的电子占有7种能量不同的原子轨道.
(2)e、f、g、h四种元素形成的离子半径由大到小顺序为O2->F->Na+>Mg2+(用离子符号表示)
(3)单质d与单质a反应的产物的分子中中心原子的杂化形式为sp3,该分子是极性(填“极性”或“非极性”)分子.
(4)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:基态原子中电子获得能量跃迁到激发态,电子从能量较高的轨道跃迁到能力较低的轨道时,以光(子)的形式释放能量.
(5)o、p两元素的部分电离能数据列于下表:
| 元素 | O | p | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(6)a、d、e可以形成一种盐,此盐的组成中a、d、e元素的原子个数比为4:2:3,此盐的化学式为NH4NO3,含有的化学键为离子键、共价键、配位键.
| A. | K+、CO32-、HS-、S2-、Al3+、AlO2- | B. | MnO4-、Na+、SO42-、K+、Cl- | ||
| C. | SO42-、Ag+、SO32-、S2-、AlO2-、K+ | D. | Fe3+、Cl-、H+、NO3- |
①气态氢化物的稳定性 ②最高化合价 ③第一电离能 ④电负性.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
 .
. ,Y的结构式为
,Y的结构式为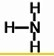 .
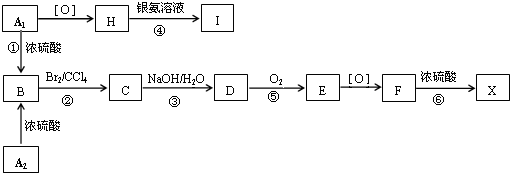
.
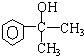 ;F
;F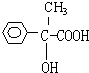 .
.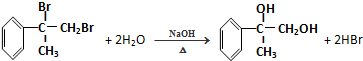 ;
; .
.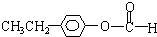 、
、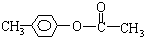 、
、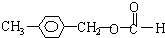 、
、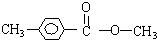 .
.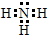 NaOH
NaOH HCl
HCl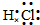 Cl2
Cl2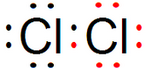 MgCl2
MgCl2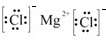 NaCl
NaCl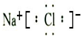 N2
N2 H2O
H2O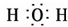 .
.