题目内容
【题目】过渡金属元素在日常生活中有广泛的应用。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为 __________;基态 Mn原子核外有____种运动状态不同的电子,M层的电子云有_______种不同的伸展方向。
(2)第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是 ____________________________________
(3)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒__________(写出一种),K3[Co(NO2)6]中存在的作用力有___________a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
(4)锰的一种配合物的化学式为 Mn(BH4)2(THF)3,BH4-的空间构型为____________
(5)FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。
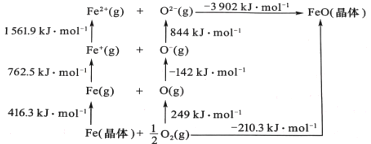
可知,O原子的第一电子亲和能为 ________kJmol-1,FeO晶格能为________kJmol-1。
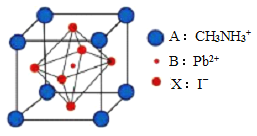
(6)铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为_______________,已知该晶体的密度为ρgcm-3,NA是阿伏伽德罗常数的值,则晶胞参数为_________pm
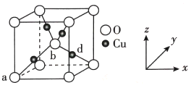
(列出计算式即可)
【答案】3d34s2 25 9 Ga:[Ar]3d104s24p1、Zn:[Ar]3d104s2,Zn:3d104s2,3d全满,能量低,稳定,难失电子,因此Ga的第一电离能明显低于Zn O3 a b c d 正四面体形 142 3902 ![]()
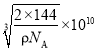
【解析】
⑴钒是23号元素,基态钒原子排布式为1s22s22p63s23p63d34s2;一个电子就是一种运动状态的电子;M层上能级有3s、3p、3d;
⑵从原子结构和3d能级全满角度分析;
⑶根据价电子N-=O,书写等电子体,NO2-含有σ键和π键,配离子[Co(NO2)6]3存在配位键,配离子[Co(NO2)6]3与K+形成离子键;
⑷计算BH4-的价层电子对数,根据价层电子互斥理论模型来写空间构型;
⑸第一电子亲和能为气态基态电中性基态原子获得一个电子变为气态一价负离子放出的能量;晶格能是指气态离子形成1mol离子晶体所释放的能量;
⑹d点在体对角线的四分之一处,与a点相对的位置,因此得d的坐标参数,根据晶体结构得到Cu、O个数和化学式,根据体积公式计算体积,再得晶胞参数。
⑴钒是23号元素,基态钒原子排布式为1s22s22p63s23p63d34s2,其价层电子的排布式为 3d34s2;一个电子就是一种运动状态的电子,因此基态Mn原子核外有25种运动状态不同的电子,M层上能级有3s、3p、3d,因此M层的电子云有9种不同的伸展方向,故答案为:3d34s2;25;9;
⑵第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,从原子结构角度分析,其原因是Ga:[Ar]3d104s24p1、Zn:[Ar]3d104s2,Zn:3d104s2,3d全满,能量低,稳定,难失电子,因此Ga的第一电离能明显低于Zn,故答案为:Ga:[Ar]3d104s24p1、Zn:[Ar]3d104s2,Zn:3d104s2,3d全满,能量低,稳定,难失电子,因此Ga的第一电离能明显低于Zn;
⑶NO2-与钴盐形成的配离子[Co(NO2)6]3可用于检验 K+的存在。根据价电子N-=O,因此与NO2-互为等电子体的微粒O3,K3[Co(NO2)6]中NO2-含有σ键和π键,配离子[Co(NO2)6]3存在配位键,配离子[Co(NO2)6]3与K+形成离子键,因此K3[Co(NO2)6]中的作用力有a b c d,故答案为:O3;a b c d;
⑷BH4-的价层电子对数为![]() ,价层电子互斥理论模型为四面体形,空间构型为正四面体形,故答案为:正四面体形;
,价层电子互斥理论模型为四面体形,空间构型为正四面体形,故答案为:正四面体形;
⑸第一电子亲和能为气态基态电中性基态原子获得一个电子变为气态一价负离子放出的能量,因此O原子的第一电子亲和能为142 kJ·mol1,晶格能是指气态离子形成1mol离子晶体所释放的能量,因此FeO晶格能为3902 kJ·mol1,故答案为:142;3902;
⑹d点在体对角线的四分之一处,与a点相对的位置,因此d的坐标参数为![]() ,根据晶体结构得到Cu有4个,O有
,根据晶体结构得到Cu有4个,O有![]() ,因此化学式为Cu2O,根据体积公式得到
,因此化学式为Cu2O,根据体积公式得到 ,则晶胞参数为
,则晶胞参数为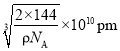 ,故答案为:
,故答案为:![]() ;
;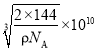 。
。

 名校课堂系列答案
名校课堂系列答案