题目内容
13.下列化学用语的书写正确的是( )| A. | 氯分子的电子式 Cl:Cl | B. | 氢分子的电子式 H:H | ||
| C. | 氯化镁的电子式 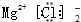 | D. | 氯化钠的电子式 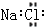 |
分析 A.氯原子未成键的孤对电子未画出;
B.氢原子之间形成1对共用电子对;
C.电子式中氯离子不能合并书写,应分布在镁离子周围;
D.氯化钠是离子化合物,由钠离子与氯离子构成.
解答 解:A.氯原子未成键的孤对电子未画出,氯气电子式为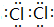 ,故A错误;
,故A错误;
B.氢原子之间形成1对共用电子对,电子式为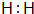 ,故B正确;
,故B正确;
C.电子式中氯离子不能合并书写,应分布在镁离子周围,氯化镁电子式为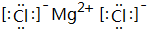 ,故C错误;
,故C错误;
D.氯化钠是离子化合物,由钠离子与氯离子构成,氯化钠电子式为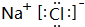 ,故D错误,
,故D错误,
故选B.
点评 本题考查电子式书写,比较基础,侧重对基础知识的巩固,注意离子化合物和共价化合物或多原子分子电子式书写区别,易错选项是A,在多原子分子中易漏掉某些孤电子对.

练习册系列答案
相关题目
3.短周期元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列推断正确的是( )
| A. | 原子半径:W>X>Z>Y | B. | 离子半径:Y>Z>X>W | ||
| C. | a+2=c-2 | D. | 热稳定性:H2Y>HZ |
4.下列实验及操作能够达到预期实验目的是( )
| A. | 用广泛pH试纸测得某溶液的pH=6.7 | |
| B. | 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 | |
| C. | 可以选用氯水、四氯化碳来检验Cl-、Br-、I- | |
| D. | 在洁净的试管中加入1mL AgNO3溶液,再加入过量浓氨水,振荡制成银氨溶液 |
1.下列化合物分子中一定既含σ键又含π键的是( )
| A. | C2H4 | B. | HClO | C. | NH3 | D. | H2O2 |
8.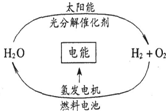 目前,科学家提出了一种经济而且理想的获得氢能源的循环体系(如右图).关于此循环体系,下列说法中错误的是( )
目前,科学家提出了一种经济而且理想的获得氢能源的循环体系(如右图).关于此循环体系,下列说法中错误的是( )
 目前,科学家提出了一种经济而且理想的获得氢能源的循环体系(如右图).关于此循环体系,下列说法中错误的是( )
目前,科学家提出了一种经济而且理想的获得氢能源的循环体系(如右图).关于此循环体系,下列说法中错误的是( )| A. | 燃料电池能够使化学反应产生的能量转化为电能 | |
| B. | 在此循环中发生了反应:2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ | |
| C. | 该氢能源的循环体系能够实现太阳能转化为电能 | |
| D. | 目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂 |
5.在一定温度下,可逆反应A(g)+3B(g)?2C(g),在密闭容器中反应,达到平衡状态的标志是( )
(1)C的生成速率与C的分解速率相等;(2)单位时间生成amol A,同时生成3amol B;(3)A、B、C的浓度不再变化;(4)混合气体的总压强不再变化;(5)速率V(A):V(B):V(C)=1:3:2;(6)条件一定,混和气体的平均相对分子质量不再变化;(7)A、B、C的分子数目比为1:3:2.
(1)C的生成速率与C的分解速率相等;(2)单位时间生成amol A,同时生成3amol B;(3)A、B、C的浓度不再变化;(4)混合气体的总压强不再变化;(5)速率V(A):V(B):V(C)=1:3:2;(6)条件一定,混和气体的平均相对分子质量不再变化;(7)A、B、C的分子数目比为1:3:2.
| A. | (1)(2)(4)(7) | B. | (2)(3)(5)(6) | C. | (1)(3)(4)(6) | D. | (1)(3)(5)(7) |
2.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol/L Na2CO3溶液中的Na+ 数目为2NA | |
| B. | 7.8 g Na2O2所含离子总数为0.4 NA | |
| C. | 1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA电子 | |
| D. | 34 g OH-中含质子数20NA |