题目内容
4.下列实验及操作能够达到预期实验目的是( )| A. | 用广泛pH试纸测得某溶液的pH=6.7 | |
| B. | 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 | |
| C. | 可以选用氯水、四氯化碳来检验Cl-、Br-、I- | |
| D. | 在洁净的试管中加入1mL AgNO3溶液,再加入过量浓氨水,振荡制成银氨溶液 |
分析 A.pH试纸测定溶液的pH为整数;
B.滴定管洗净后经蒸馏水润洗,再用标准液润洗;
C.氯气和氯离子不反应,氯气和溴离子反应生成溴单质,溶液呈橙色;氯气和碘离子反应生成碘单质,碘溶液呈紫色;
D.银氨溶液配制方法为:在洁净的试管中加入2% AgNO3溶液1~2mL,逐滴加入2%稀NH3水,Ag++NH3•H2O═AgOH↓+NH4+,边滴边振荡,至沉淀恰好溶解时为止.
解答 解:A.pH试纸测定溶液的pH为整数而没有小数,故A错误;
B.滴定管洗净后经蒸馏水润洗,再用标准液润洗,否则会导致量取的溶液浓度偏低,故B错误;
C.氯气和氯离子不反应,氯气和溴离子反应生成溴单质,溶液呈橙色;氯气和碘离子反应生成碘单质,碘溶液呈紫色,反应现象不同,可以鉴别,故C正确;
D.银氨溶液配制方法为:在洁净的试管中加入2% AgNO3溶液1~2mL,逐滴加入2%稀NH3水,Ag++NH3•H2O═AgOH↓+NH4+,边滴边振荡,至沉淀恰好溶解时为止,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器的洗涤和使用、pH的测定、离子检验、溶液配制等知识点,侧重考查基本操作、实验原理等知识点,明确仪器的使用方法、操作规范性即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
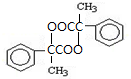
14.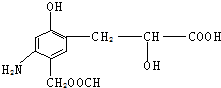 分析下列有机物的结构,判断该有机物可能发生的反应类型:( )
分析下列有机物的结构,判断该有机物可能发生的反应类型:( )
①加成反应 ②消去反应 ③取代反应 ④水解反应 ⑤中和反应 ⑥显色反应 ⑦氧化反应.
 分析下列有机物的结构,判断该有机物可能发生的反应类型:( )
分析下列有机物的结构,判断该有机物可能发生的反应类型:( )①加成反应 ②消去反应 ③取代反应 ④水解反应 ⑤中和反应 ⑥显色反应 ⑦氧化反应.
| A. | 除④外其余都有 | B. | 全部 | C. | 只④⑤⑥⑦ | D. | 只①③⑤⑥⑦ |
12.下列各装置中铜电极上能产生气泡的是( )
| A. |  | B. |  | ||
| C. | 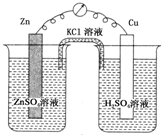 | D. | 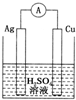 |
19.下列排列顺序错误的是( )
| A. | 原子半径:O<S<Na | B. | 稳定性:HF>H2S>HCl | ||
| C. | 酸性:H2SiO3<H2CO3<HNO3 | D. | 碱性:Al(OH)3<Mg(OH)2<NaOH |
13.下列化学用语的书写正确的是( )
| A. | 氯分子的电子式 Cl:Cl | B. | 氢分子的电子式 H:H | ||
| C. | 氯化镁的电子式 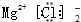 | D. | 氯化钠的电子式 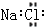 |
14.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
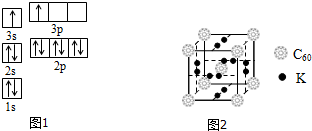
(1)某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)ACl2分子中A的杂化类型为sp杂化.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确不正确(填“正确”或“不正确”),并阐述作出判断的理由:C60是分子晶体,熔化时不需破坏化学键.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4S1,该物质中K原子和C60分子的个数比为3:1.
(5)C、Si、N原子电负性由大到小的顺序是N>C>Si,NCl3分子的VSEPR模型为正四面体.
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

(2)ACl2分子中A的杂化类型为sp杂化.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确不正确(填“正确”或“不正确”),并阐述作出判断的理由:C60是分子晶体,熔化时不需破坏化学键.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4S1,该物质中K原子和C60分子的个数比为3:1.
(5)C、Si、N原子电负性由大到小的顺序是N>C>Si,NCl3分子的VSEPR模型为正四面体.
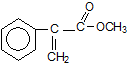
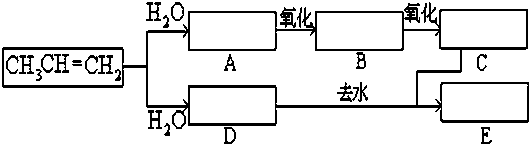
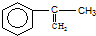 出发合成A,其合成路线如下:已知:A在酸性条件下水解生成有机物B和甲醇.
出发合成A,其合成路线如下:已知:A在酸性条件下水解生成有机物B和甲醇.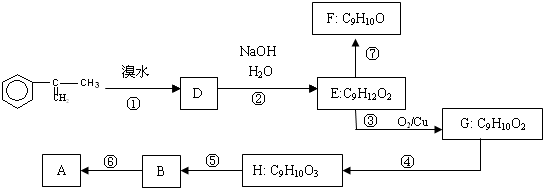
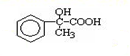 .
.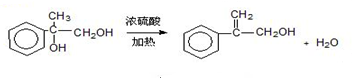 .
. .
.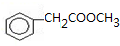 .
.