题目内容
3.向某硝酸银溶液中逐滴加入1.1g•mL-1的盐酸,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸的质量相等,求盐酸的质量分数和物质的量浓度.分析 发生反应:AgNO3+HCl═AgCl↓+HNO3,过滤所得沉淀的质量恰好与盐酸的质量相等,设AgCl质量为143.5g,其物质的量为1mol,由氯离子守恒,则HCl物质的量为1mol,可知HCl质量为36.5g,质量分数=$\frac{m(溶质)}{m(溶液)}$×100%,根据c=$\frac{1000ρω}{M}$计算物质的量浓度.
解答 解:发生反应:AgNO3+HCl═AgCl↓+HNO3,过滤所得沉淀的质量恰好与盐酸的质量相等,设AgCl质量为143.5g,其物质的量为$\frac{143.5g}{143.5g/mol}$=1mol,由氯离子守恒,则HCl物质的量为1mol,可知HCl质量为1mol×36.5g/mol=36.5g,
故盐酸溶液质量分数为$\frac{36.5g}{143.5g}$×100%=25.44%
物质的量浓度为$\frac{1000×1.1×\frac{36.5}{143.5}}{36.5}$mol/L=7.67mol/L,
答:盐酸的质量分数为25.44%,物质的量浓度为7.67mol/L.
点评 本题考查溶液浓度计算,涉及物质的量浓度、质量分数,注意特殊值法的运用,注意理解物质的量浓度与质量分数关系.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
13.下列化学用语的书写正确的是( )
| A. | 氯分子的电子式 Cl:Cl | B. | 氢分子的电子式 H:H | ||
| C. | 氯化镁的电子式 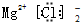 | D. | 氯化钠的电子式 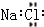 |
14.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
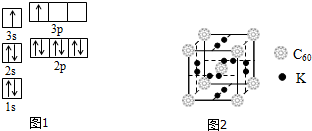
(1)某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)ACl2分子中A的杂化类型为sp杂化.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确不正确(填“正确”或“不正确”),并阐述作出判断的理由:C60是分子晶体,熔化时不需破坏化学键.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4S1,该物质中K原子和C60分子的个数比为3:1.
(5)C、Si、N原子电负性由大到小的顺序是N>C>Si,NCl3分子的VSEPR模型为正四面体.
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

(2)ACl2分子中A的杂化类型为sp杂化.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确不正确(填“正确”或“不正确”),并阐述作出判断的理由:C60是分子晶体,熔化时不需破坏化学键.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4S1,该物质中K原子和C60分子的个数比为3:1.
(5)C、Si、N原子电负性由大到小的顺序是N>C>Si,NCl3分子的VSEPR模型为正四面体.
18.某氯化镁溶液的密度为d g•cm-3,其中镁离子的质量分数为ω,a mL该溶液的Cl-的物质的量为( )
| A. | $\frac{adω}{24}$mol | B. | $\frac{dω}{24a}$mol | C. | $\frac{adω}{22400}$mol | D. | $\frac{adω}{12}$mol |
8.下列离子方程式书写不正确的是( )
| A. | NaOH和稀H2SO4:OH-+H+═H2O | |
| B. | NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-═NH3↑+H2O | |
| C. | 碳酸钠溶液中通入少量CO2:CO32-+CO2+H2O═2HCO3- | |
| D. | NaHCO3和H2SO4反应:HCO3-+H+═H2O+CO2↑ |
15.等质量的两份铜粉分别与足量浓硫酸和浓硝酸充分反应时,消耗的硫酸和硝酸的物质的量分别为a mol和b mol,下列判断正确的是( )
| A. | a>b | B. | a<2b | C. | a=b | D. | 2a=b |
17.可以证明乙醇分子中有一个氢原子与另外氢原子不同的方法是( )
| A. | 1 mol乙醇燃烧生成3 mol水 | |
| B. | 乙醇可以制饮料 | |
| C. | 1 mol乙醇跟足量的Na作用得0.5 mol H2 | |
| D. | 乙醇代替汽油做燃料,污染小,更环保 |
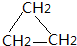 .
.