题目内容
(15分)锌锰干电池所含的汞、酸或碱等在废弃后进入环境中将造成严重危害。对废旧电池进行资源化处理显得非常重要。某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源。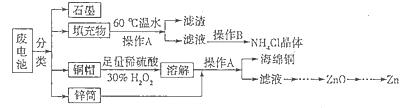
(1)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为_________________________________________________________。
(2)填充物用60℃温水溶解,目的是加快溶解速率,但必须控制温度不能太高,其原因是___________。
(3)操作A的名称为_____________ 。
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止。其主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4=2MnSO4+4CO2↑+6H2O。
①当1 mol MnO2参加反应时,共有___________mol电子发生转移。
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出其反应的化学方程式:________________。
(5)铜帽溶解时加入H2O2的目的是_______________________________(用化学方程式表示)。铜帽溶解完全后,可采用_____________方法除去溶液中过量的H2O2。
(6)锌锰干电池所含的汞可用KMnO4溶液吸收。在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如下图所示:
根据上图可知:
①pH对Hg吸收率的影响规律是__________________________________________________.
②在强酸性环境下Hg的吸收率高的原因可能是_____________________________________.
(1)Zn+2OH--2e-=Zn(OH)2 (2)温度过高氯化铵受热分解 (3)过滤
(4)①4 ②2MnO(OH)+6HCl(浓)  2MnCl2+Cl2↑+4H2O
2MnCl2+Cl2↑+4H2O
(5)Cu+H2O2+H2SO4=CuSO4+2H2O 加热
(6)①随pH升高,汞的吸收率先降低后增加 ② KMnO4在酸性条件下氧化性强
解析试题分析:(1)根据已知条件可知该电池中的负极的电极式是Zn+2OH--2e-=Zn(OH)2。(2)为加快溶解速率填充物要用温水溶解,但温度不能太高,否则氯化铵受热分解。(3)把不溶性的固体与可溶性固体分离的操作是过滤。(4)①当1 mol MnO2参加反应时,共有4molC原子有反应前的+3价变为+4价。所以转移电子4mol。②根据电子守恒及质量守恒定律可得MnO(OH)与浓盐酸在加热条件下反应的化学方程式为2MnO(OH)+6HCl(浓)  2MnCl2+Cl2↑+4H2O。(5)铜帽溶解时加入H2O2的目的是为了溶解Cu单质。反应的方程式为Cu+H2O2+H2SO4=CuSO4+2H2O。铜帽溶解完全后,溶液中含有过量的H2O2。由于H2O2不稳定,受热容易发生分解反应产生氧气和水。所以可采用加热的方法除去溶液中过量的H2O2。(6)根据上图可知:①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率逐渐降低,当溶液的pH>11后又增加。即:先降低后升高。②在强酸性环境下Hg的吸收率高的原因可能是强酸性环境中KMnO4的氧化性强。
2MnCl2+Cl2↑+4H2O。(5)铜帽溶解时加入H2O2的目的是为了溶解Cu单质。反应的方程式为Cu+H2O2+H2SO4=CuSO4+2H2O。铜帽溶解完全后,溶液中含有过量的H2O2。由于H2O2不稳定,受热容易发生分解反应产生氧气和水。所以可采用加热的方法除去溶液中过量的H2O2。(6)根据上图可知:①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率逐渐降低,当溶液的pH>11后又增加。即:先降低后升高。②在强酸性环境下Hg的吸收率高的原因可能是强酸性环境中KMnO4的氧化性强。
考点:考查废电池中的各种资源回收利用及混合物的分离方法、物质的性质、方程式的书写的知识。

蓝铜矿主要含xCuCO3·yCu(OH)2,还含有少量Fe的化合物,工业上以蓝铜矿为原料制备Cu、CaCO3和CuSO4.5H2O。具体方法步骤如下: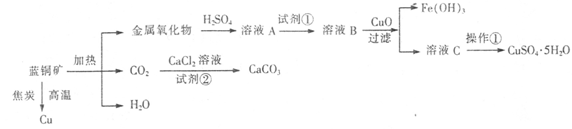
已知:
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
(1)蓝铜矿的主要成分与焦炭高温条件可以生成铜、二氧化碳和水,写出该反应的化学方程式
。
(2)从下列所给试剂中选择:实验步骤中试剂①为 (填代号)。
a.KMnO4 b.K2Cr2O7 c.H2O2 d.氯水
(3)在溶液B中加入CuO的作用是调节溶液pH,则pH的范围为 。
(4)由溶液C获得CuSO4.5H2O,需要经过加热蒸发浓缩、冷却结晶、过滤等操作,加热蒸发至 时停止加热。
(5)制备CaCO3时,应向CaCl2溶液中先通人(或加入)试剂②,则试剂②可以是
(填代号);
a.氨水 b.盐酸 c.水蒸气 d.NaOH溶液
如果不加人试剂②,则CaCl2溶液不能与CO2反应生成CaCO3,请依据难溶电解质的沉淀溶解平衡原理分析可能的原因 。
(6)为确定试剂①的用量,需测定溶液A中Fe2+的浓度。实验操作为:准确量取20.00mL 溶液A于锥形瓶中,用0.01200 mol/L的酸性KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液15.00 mL,则溶液A中Fe2+的浓度为 。
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下: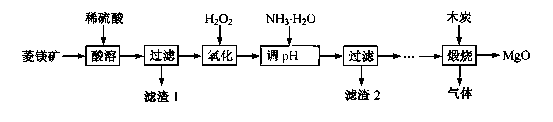
生成氢氧化物沉淀的pH
| | Mg(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 9.4 | 6.3 | 1.5 |
| 完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加氨水调节溶液的PH范围为 。
(3)滤渣2 的成分是 (填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C
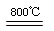 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑MgSO4+C
 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑ MgSO4+3C
 MgO+S↓+3CO↑
MgO+S↓+3CO↑利用下图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体是 (填化学式)。
②B中盛放的溶液是 (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硫酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: 。
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为(MgCO3,舍少量FeCO3)为原料制备高纯氧化镁的实验流程如下: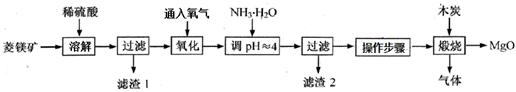
(1)通入O2氧化时,发生反应的离子方程式为____________________。
(2)滤渣2的成分是_________(填化学式)
(3)流程图中“操作步骤”为 、过滤等操作,得到MgSO4·7H2O晶体。对MgSO4·7H2O晶体直接加热 (填“能”或“不能”)得到无水MgSO4固体。
(4)长时间加热MgCO3悬浊液后生成Mg(OH)2,该反应的化学方程式为 。
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
| pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
(6)煅烧过程存在以下反应:
2MgSO4+C
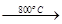 2MgO+2SO2↑+CO2↑; MgSO4+C
2MgO+2SO2↑+CO2↑; MgSO4+C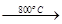 MgO+SO2↑+CO↑;
MgO+SO2↑+CO↑;MgSO4+3C
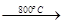 MgO+S↑+3CO↑。
MgO+S↑+3CO↑。①若在实验室中煅烧硫酸镁,需要的仪器除酒精灯、三脚架以外,还需要 。
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
②用下列实验装置检验煅烧产生的气体中含有SO2、CO2气体(加热装置略去,部分装置可以重复使用)。
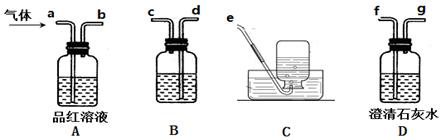
正确的连接顺序是a→b→ (按接口连接)。B中盛放的试剂是 ,确定存在二氧化碳气体的实验现象是 。