题目内容
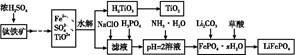
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为(MgCO3,舍少量FeCO3)为原料制备高纯氧化镁的实验流程如下: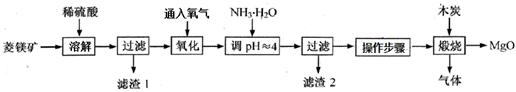
(1)通入O2氧化时,发生反应的离子方程式为____________________。
(2)滤渣2的成分是_________(填化学式)
(3)流程图中“操作步骤”为 、过滤等操作,得到MgSO4·7H2O晶体。对MgSO4·7H2O晶体直接加热 (填“能”或“不能”)得到无水MgSO4固体。
(4)长时间加热MgCO3悬浊液后生成Mg(OH)2,该反应的化学方程式为 。
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
| pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
(6)煅烧过程存在以下反应:
2MgSO4+C
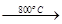 2MgO+2SO2↑+CO2↑; MgSO4+C
2MgO+2SO2↑+CO2↑; MgSO4+C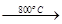 MgO+SO2↑+CO↑;
MgO+SO2↑+CO↑;MgSO4+3C
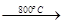 MgO+S↑+3CO↑。
MgO+S↑+3CO↑。①若在实验室中煅烧硫酸镁,需要的仪器除酒精灯、三脚架以外,还需要 。
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
②用下列实验装置检验煅烧产生的气体中含有SO2、CO2气体(加热装置略去,部分装置可以重复使用)。
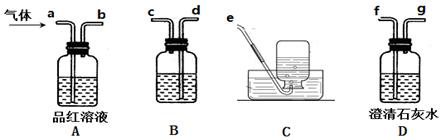
正确的连接顺序是a→b→ (按接口连接)。B中盛放的试剂是 ,确定存在二氧化碳气体的实验现象是 。
(1)4Fe2++O2+4H+=4Fe3++2 H2O(2分) (2)Fe(OH)3(2分)
(3)蒸发浓缩、冷却结晶 (2分,少选一个扣1分) 能 (1分)
(4)MgCO3+H2O= Mg(OH)2+CO2↑(2分)
(5)蓝色(2分)
(6)①B C (2分,少选一个扣1分)
②dcabfge(或dcfge)(2分,少选、错选不得分) 酸性高锰酸钾溶液(2分)
后A中品红不褪色,澄清石灰水变浑浊(或B中颜色变浅,澄清石灰水变浑浊)(2分)
解析试题分析:(1)菱镁矿与硫酸反应生成Fe2+,通入氧气,把Fe2+氧化为Fe3+,离子方程式为:4Fe2++O2+4H+=4Fe3++2 H2O
(2)调节pH至4,Fe3+转化为Fe(OH)3,所以滤渣2的成分是Fe(OH)3。
(3)从MgSO4溶液得到MgSO4·7H2O晶体,先加热蒸发水分,使MgSO4溶液浓度变大,然后降温,MgSO4的溶解度减小,析出MgSO4·7H2O晶体,所以流程图中“操作步骤”为:蒸发浓缩、冷却结晶;将MgSO4?7H2O晶体直接加热会造成结晶水脱去,硫酸镁较稳定,可以稳定存在,所以对MgSO4·7H2O晶体直接加热能得到无水MgSO4固体。
(4)长时间加热MgCO3悬浊液后生成Mg(OH)2,化学方程式为:MgCO3+H2O= Mg(OH)2+CO2↑
(5)根据Mg(OH)2的溶度积Ksp=5.6×10-12,可得c(Mg2+)?c2(OH?)= 5.6×10-12,c (OH?)="2" c(Mg2+),可得c3(OH?)=2.246×10-11,可估算出pH>10,故溶液呈现蓝色。
(6)①煅烧固体物质的仪器为坩埚,坩埚需要在放在泥三角上加热,故答案为BC。
②B中溶液的作用为除去SO2,防止干扰CO2的检验,所以B中溶液为:酸性高锰酸钾溶液;首先连接dc,连接ab,品红的作用是证明SO2已完全被除去,在连接fg,用澄清石灰水检验CO2,所以连接顺序为:dcabfge(或dcfge);后A中品红不褪色或B中颜色变浅,,说明SO2已完全除去,澄清石灰水变浑浊,则可证明气体中含CO2.
考点:本题考查化学流程的分析、方程式的书写、基本操作和基本仪器、溶度积的计算、气体的检验。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上黏附着白色物质。
【提出假设】
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:白色物质是Na2O和Na2CO3的混合物。
【设计实验方案验证假设】 该小组对燃烧后的白色产物
进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | |
| | ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【思考与交流】
(1)甲同学认为方案1得到的结论不正确,其理由是 。
(2)乙同学认为方案2得到的结论正确,白色物质为 。
(3)通过方案1和方案2的实验,你认为上述三个假设中, 成立。你的理由是 。
(4)钠在二氧化碳中燃烧的化学方程式为 。
(5)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点?并简述理由: 。
为探究某抗酸药X的组成,进行如下实验:
查阅资料:
①抗酸药X可能的组成可以表示为:MgmAln(OH)p(CO3)q(SiO3)r(m、n、p、q、r为≥0的整数)。
② 在pH=5.0时沉淀完全;
在pH=5.0时沉淀完全; 在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
实验过程:
| 步骤 | 实验操作 | 实验现象 |
| I | 向X的粉末中加入过量盐酸 | 产生气体A,得到无色溶液 |
| II | 向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,过滤 | 生成白色沉淀B |
| III | 向沉淀B中加过量NaOH溶液 | 沉淀全部溶解 |
| IV | 向II得到的滤液中滴加NaOH溶液,调节pH至12 | 生成白色沉淀C |
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是 。
(2)II中生成B反应的离子方程式是 。
(3)III中B溶解反应的离子方程式是 。
(4)沉淀C的化学式是 。
(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,则X的化学式是 。



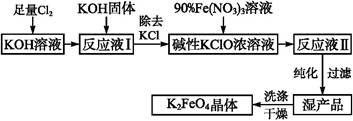
 KCl+KClO+H2O(条件:温度较低)
KCl+KClO+H2O(条件:温度较低) ;② 。
;② 。