题目内容
【题目】新冠疫情期间使用大量的消毒剂,其中二氧化氯(ClO2)与亚氯酸钠(NaClO2)都具有强氧化性。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组利用如下装置由二氧化氯制备NaClO2·3H2O,并探究其性质。

查阅资料:
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
回答下列问题:
(1)仪器a的名称_________。
(2)装置A中发生反应的化学方程式:________。
(3)如果撤去C装置中的冷水浴,导致产品中可能混有的杂质是_______。
(4)若要从装置C反应后的溶液获得无水NaClO2晶体的操作步骤如下,请完成下列操作步骤③的内容。
①减压,55℃蒸发结晶; ②趁热过滤;③_________; ④低于60℃干燥,得到成品。
(5)写出装置C反应的离子方程式________。
(6)实验结束后,继续通入一段时间N2的目的是________。
(7)利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2![]() =
=![]() +2I-)取样品0.6000 g配制成250 mL溶液,从中取出25.0 mL加入足量KI固体和适量稀硫酸,再滴加几滴淀粉溶液,然后用0.0600 mol/L Na2S2O3标准溶液滴定,当出现________(填实验现象),达到滴定终点,共消耗该标准溶液25.00 mL,经计算该试样中NaClO2·3H2O的百分含量为______(结果保留3位有效数字)。
+2I-)取样品0.6000 g配制成250 mL溶液,从中取出25.0 mL加入足量KI固体和适量稀硫酸,再滴加几滴淀粉溶液,然后用0.0600 mol/L Na2S2O3标准溶液滴定,当出现________(填实验现象),达到滴定终点,共消耗该标准溶液25.00 mL,经计算该试样中NaClO2·3H2O的百分含量为______(结果保留3位有效数字)。
【答案】分液漏斗 2NaClO3 + H2SO4 + Na2SO3=== 2Na2SO4 + 2ClO2 ↑ + H2O NaClO3 、 NaCl 用38℃~60℃热水洗涤 2ClO2+H2O2+2OH-===2![]() +2H2O+O2 将装置内残留的ClO2全部排出,提高产率 溶液由蓝色褪为无色,且30秒内不复原 90.3%
+2H2O+O2 将装置内残留的ClO2全部排出,提高产率 溶液由蓝色褪为无色,且30秒内不复原 90.3%
【解析】
由题中信息可知,A装置中制备二氧化氯气体,该气体经安全瓶B进入C装置,在碱性条件下二氧化氯被双氧水还原为亚氯酸钠,D装置为尾气处理装置。有关纯度的计算可以根据反应的关系式进行。
(1)由仪器a的构造可知其为分液漏斗。
(2)装置A中NaClO3、H2SO4、Na2SO3发生反应生成ClO2,该反应的化学方程式为2NaClO3+ H2SO4+ Na2SO3=== 2Na2SO4 + 2ClO2↑ + H2O。
(3)由题中信息可知,高于60℃时NaClO2分解成NaClO3和NaCl,所以如果撤去C装置中的冷水浴,导致产品中可能混有的杂质是NaClO3 、 NaCl。
(4) 由题中信息可知,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl,因此,若要从装置C反应后的溶液获得无水NaClO2晶体的操作步骤如下:①减压,55℃蒸发结晶; ②趁热过滤;③用38℃~60℃热水洗涤(除去其中的可溶性杂质); ④低于60℃干燥,得到成品。
(5)装置C 中,在碱性条件下二氧化氯被双氧水还原为亚氯酸钠,该反应的离子方程式为2ClO2+H2O2+2OH-===2![]() +2H2O+O2。
+2H2O+O2。
(6)实验结束后,装置内还有残留的ClO2,若不排出,则产品的产率会降低,因此继续通入一段时间N2的目的是:将装置内残留的ClO2全部排出,提高产率。
(7)取样品0.6000 g配制成250 mL溶液,从中取出25.0 mL加入足量KI固体和适量稀硫酸,碘离子被亚氯酸钠氧化为碘,再滴加几滴淀粉溶液作指示剂,溶液变蓝,然后用0.0600 mol/L Na2S2O3标准溶液滴定,反应完成后溶液的蓝色褪去,因此,当出现溶液由蓝色褪为无色,且30秒内不复原,达到滴定终点。若共消耗该标准溶液25.00 mL,由ClO2-+4I-+4H+=Cl-+2I2+2H2O、I2+2![]() =
=![]() +2I-,可以得到关系式NaClO2·3H2O~2I2~4
+2I-,可以得到关系式NaClO2·3H2O~2I2~4![]() ,则25.0 mL 样品溶液中,n(NaClO2·3H2O)=
,则25.0 mL 样品溶液中,n(NaClO2·3H2O)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() 25.0010-3L0.0600 mol/L=
25.0010-3L0.0600 mol/L=![]() 0.0000600mol,该试样中NaClO2·3H2O的百分含量为
0.0000600mol,该试样中NaClO2·3H2O的百分含量为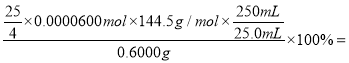 90.3%。
90.3%。

【题目】过氧化氢是重要的化工产品,广泛应用于化学合成、医疗消毒等领域。
(1)过氧化氢的电子式为_____________。
(2)工业上电解硫酸氢盐溶液得到过二硫酸盐(![]() ),过二硫酸盐水解生成H2O2溶液和硫酸氢盐,生成的硫酸氢盐可以循环使用。电解硫酸氢盐溶液时阳极的电极反应式为_______。写出过二硫酸盐水解的离子方程式________。
),过二硫酸盐水解生成H2O2溶液和硫酸氢盐,生成的硫酸氢盐可以循环使用。电解硫酸氢盐溶液时阳极的电极反应式为_______。写出过二硫酸盐水解的离子方程式________。
(3)298K时,实验测得反应![]() 在不同浓度时的化学反应速率如表:
在不同浓度时的化学反应速率如表:
实验编号 | 1 | 2 | 3 | 4 | |
c(HI) /mol﹒L-1 | 0.100 | 0.200 | 0.300 | 00.100 | 0.100 |
c(H2O2)/mol﹒L-1 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
v//mol﹒L-1﹒s-1 | 0.007 60 | 0.015 3 | 0.022 7 | 0.015 1 | 0.022 8 |
已知速率方程为![]() ,其中k为速率常数。
,其中k为速率常数。
根据表中数据判断:a=_______,b=________。
(4)“大象的牙膏”实验是将浓缩的过氧化氢与肥皂液混合,再滴加少量碘化钾溶液,即可观察到泡沫状物质像喷泉一样喷涌而出。反应中H2O2的分解机理为:
![]() 慢
慢
![]() 快
快
此反应过程中无催化剂和有催化剂的能量变化关系图像如图所示:

则表示慢反应的曲线是__________(填“a”或“b”)。
1mol H2O2分解放出热量98 kJ,则H2O2分解的热化学方程式为_________________。
(5)某科研团队研究![]() 体系(其中
体系(其中![]() )氧化苯乙烯制取苯甲醛,反应的副产物主要为苯甲酸和环氧苯乙烷。一定条件下,测得一定时间内温度对氧化反应的影响如图:
)氧化苯乙烯制取苯甲醛,反应的副产物主要为苯甲酸和环氧苯乙烷。一定条件下,测得一定时间内温度对氧化反应的影响如图:

注:■苯乙烯转化率 ●苯甲醛选择性
①80℃时苯乙烯的转化率有所降低,其原因可能是_______。
②结合苯乙烯的转化率,要获得较高的苯甲醛产率,应该选择的温度为_______。