题目内容
【题目】(1)写出铜原子价电子排布式:______。与铜同一周期的副族元素原子中最外层电子数与铜原子的相同的元素有________(填元素符号)。
(2)第三周期第一电离能处于Al和P之间的元素有______种。
(3)某种原子的结构示意图为![]() 。则该原子的核电荷数x取值范围为______。
。则该原子的核电荷数x取值范围为______。
(4)Cr在周期表中位于_____周期___族,属于___区,价电子排布图为______
(5)ClO4-互为等电子体的分子或离子为____。
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_____。
【答案】3d104s1 Cr 3 20≤x≤30且X不等于24和29 四 VIB d 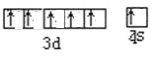 SO42-或其他合理答案 1:1
SO42-或其他合理答案 1:1
【解析】
(1)Cu原子3d、4s能级上电子为其价电子,3d能级上有10个电子、4s能级上有1个电子,其价电子排布式为3d104s1;
铜原子最外层排布为4s1,同周期外层排布为4s1,副族中d能级含有5个电子为Cr;
(2)同一周期元素,元素的第一电离能随着原子序数的增大而呈增大趋势,但同一周期中第ⅡA族元素比第ⅢA族元素的第一电离能大,第ⅤA族比第ⅥA族第一电离能大,Mg、Al、Si、P、S、Cl属于同一周期且其原子序数依次增大,但Mg属于第ⅡA元素,Al属于第ⅢA族,P属于第VA元素,S属于第ⅥA族,所Mg、Al、Si、P、S、Cl几种元素的第一电离能的大小顺序是P、S、Si、Mg、Al,所以第一电离能处于Al、P之间的元素有3种;
(3) 某种原子的结构示意图为![]() ,第三层电子数8≤y≤18,则该原子的核电荷数x取值范围为20≤x≤30,根据各能级的能量递增可知,x不等于24和29,故答案为20≤x≤30且x不等于24和29;
,第三层电子数8≤y≤18,则该原子的核电荷数x取值范围为20≤x≤30,根据各能级的能量递增可知,x不等于24和29,故答案为20≤x≤30且x不等于24和29;
(4)Cr为24号元素,在周期表中位于第四周期VIB族,属于d区,价电子排布图为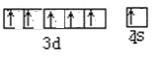 ;
;
(5)原子总数相同、价电子总数相同的微粒互为等电子体,与ClO4-互为等电子体的一种分子为CCl4,离子有SO42-;
(6)Ni与CO能形成配合物Ni(CO)4,CO中含有1个σ键,2个π键,配位键也属于共价键,也为σ键,该分子中σ键为: 1×4+4=8,π键个数为: 2×4=8,二者的比值为1:1。