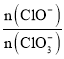题目内容
【题目】向含有淀粉的 KIO3 酸性溶液滴加 NaHSO3 溶液,溶液先变蓝后褪色。下列说法错误的是
A.溶液先变蓝的原因:2IO![]() +5HSO
+5HSO![]() =I2+5SO
=I2+5SO![]() +H2O+3H+
+H2O+3H+
B.溶液恰好褪色时 n(KIO3):n(NaHSO3)=1:3
C.还原性 I-> HSO![]() >I2
>I2
D.若向含有淀粉的 NaHSO3 溶液中滴加过量 KIO3 酸性溶液,则溶液变蓝不褪色
【答案】C
【解析】
A.溶液变成蓝色,说明有单质碘生成,即I元素化合价由+5价降低至0价,被还原,IO![]() 为氧化剂,S元素的化合价由+4价升高至+6价,被氧化,HSO
为氧化剂,S元素的化合价由+4价升高至+6价,被氧化,HSO![]() 为还原剂,反应的离子方程式为2IO
为还原剂,反应的离子方程式为2IO![]() +5HSO
+5HSO![]() =I2+5SO
=I2+5SO![]() +H2O+3H+,A选项正确;
+H2O+3H+,A选项正确;
B.溶液褪色,说明碘单质又被亚硫酸氢钠还原,离子方程式为I2+HSO![]() =2I-+SO
=2I-+SO![]() +3H+,结合A选项,可知溶液恰好褪色时n(KIO3):n(NaHSO3)=1:3,B选项正确;
+3H+,结合A选项,可知溶液恰好褪色时n(KIO3):n(NaHSO3)=1:3,B选项正确;
C.由A选项中的反应可知,还原性:HSO![]() >I2,由B选项中的反应可知,还原性HSO
>I2,由B选项中的反应可知,还原性HSO![]() >I-,又还原性I->I2,则还原性:HSO
>I-,又还原性I->I2,则还原性:HSO![]() >I->I2,C选项错误;
>I->I2,C选项错误;
D.若向含有淀粉的 NaHSO3 溶液中滴加过量KIO3酸性溶液,由于氧化性IO![]() >I2,所以不会出现I2被还原的情况,即溶液变蓝不褪色,D选项正确;
>I2,所以不会出现I2被还原的情况,即溶液变蓝不褪色,D选项正确;
答案选C。

【题目】某探究性学习小组欲用酸碱中和滴定法测定市售白醋的总酸量(g·100mL-1)。有关操作如下:
Ⅰ.实验步骤
(1)用________(填仪器名称)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴________作指示剂。
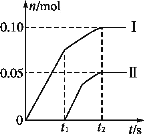
(3)读取盛装0.1000mol·L-1NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。
![]()
(4)滴定。当__________________________________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(1)处理数据可得:c(市售白醋)=________mol·L-1;市售白醋总酸量=________g·100mL-1。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是________填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
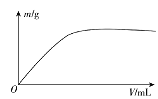
【题目】在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
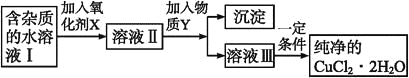
已知某温度下:Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
Fe3+ | Fe2+ | Cu2+ | |
氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂X的目的是_______________________。
(2)最适合作氧化剂X的是___________(填编号,否则不给分);写出氧化剂X参与的离子反应方程式_________。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)为了除去Fe3+,需加入物质Y_________(填化学式)调节溶液的pH值为___________。
(4)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________(填“能”或“不能”);若能,不用回答;若不能,回答该如何操作?____________________。
(5)常温下已知Fe(OH)3的Ksp=1.0×10-35,向500mL 0.2mol/L的FeCl3溶液中加入NaOH固体(溶液体积变化忽略不计)后pH=3.0,则需要加入氢氧化钠固体的质量为________g。