题目内容
19.对于达到平衡状态的可逆反应:N2+3H2?2NH3,下列有关叙述正确的是( )| A. | N2和NH3的质量分数相等 | B. | N2、H2、NH3的浓度之比为1:3:2 | ||
| C. | 反应物和生成物浓度不再发生变化 | D. | 正反应和逆反应不再进行 |
分析 化学反应达到化学平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,注意反应方程式中气体的化学计量数之和前后不等,可从压强的角度分析.
解答 解:A.达到平衡状态时,N2和NH3的质量分数不一定相等,取决于物质的起始物质的量和反应的转化程度,不能作为判断是否达到平衡状态的依据,故A错误;
B.达到平衡状态时,反应物和生成物的浓度取决于物质的起始浓度和反应的转化程度,N2、H2、NH3的浓度之比为1:3:2不能作为判断是否达到平衡状态的依据,故B错误;
C.化学反应达到化学平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,故C正确;
D.化学反应达到化学平衡状态时,正逆反应速率相等,仍在进行,故D错误.
故选C.
点评 本题考查化学平衡状态的判断,题目难度不大,本题注意化学平衡的本质为正逆反应速率相等,各物质的物质的量、浓度关系不能作为判断是否达到平衡的依据,为易错点.

练习册系列答案
相关题目
2.向AgNO3溶液中加入过量氨水,可生成[Ag(NH3)2]OH.下列说法正确的是( )
| A. | 氨气极易溶于水,所得的氨水中存在3种不同的氢键 | |
| B. | [Ag(NH3)2]+ 中含有6个σ键 | |
| C. | [Ag(NH3)2]OH所含有的化学键有离子键、极性共价键和配位键 | |
| D. | 在[Ag(NH3)2]+离子中Ag+给出孤对电子,NH3提供空轨道 |
10.哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下发生反应:N2+3H2?2NH3.下列有关说法不正确的是( )
| A. | 若2分钟达到化学平衡时N2还剩下0.4mol,则v(N2)=0.3mol/(L•min) | |
| B. | 达到化学平衡时,单位时间内每生成0.1mol的H2同时生成0.1mol的NH3 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| D. | 达到化学平衡后,若增大压强使容器体积缩小,化学反应速率将会增大 |
14.下列装置能达到实验目的是( )
| A. | 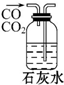 除去杂质气体CO2 | B. | 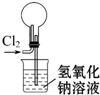 收集并吸收多余Cl2 | ||
| C. | 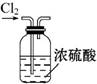 干燥Cl2 | D. |  吸收HCl制盐酸 |
4.下列装置所示的实验能达到实验目的是( )
| A. |  分离碘酒中 的碘和酒精 | B. | 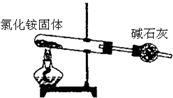 实验室制取氨气 | ||
| C. | 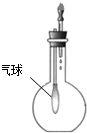 验证NH3的 溶解性 | D. | 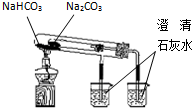 比较Na2CO3、NaHCO3的热稳定性 |
8.已知反应:A(g)+B(g)═C(g)+D(g)的能量变化如图所示,下列说法正确的是( )
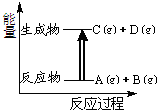

| A. | 若此反应过程中有电子转移,可设计成原电池 | |
| B. | 该反应为吸热反应 | |
| C. | A、B的键能总和小于C、D的键能总和 | |
| D. | 该反应只有在加热条件下才能进行 |
9.近段时间,朝鲜的“核危机”引起了全球的瞩目,其焦点问题就是朝鲜核电站采用轻水堆还是重水堆,重水堆核电站在发电的同时还可以生产出可供研制核武器的钚(${\;}_{94}^{239}$Pu),下列有关${\;}_{94}^{239}$PuPu的说法不正确的是( )
| A. | ${\;}_{94}^{239}$Pu含94个质子 | |
| B. | ${\;}_{94}^{239}$Pu中的中子数和质子数之差为51 | |
| C. | ${\;}_{94}^{239}$Pu中含有94个中子 | |
| D. | ${\;}_{94}^{239}$Pu具有放射性 |