题目内容
14.下列装置能达到实验目的是( )| A. | 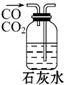 除去杂质气体CO2 | B. | 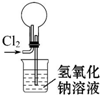 收集并吸收多余Cl2 | ||
| C. | 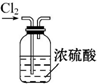 干燥Cl2 | D. | 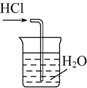 吸收HCl制盐酸 |
分析 A.除杂时导管长进短出;
B.氯气的密度比空气的密度大,且氯气易与NaOH溶液反应;
C.氯气与浓硫酸不反应,浓硫酸具有吸水性;
D.HCl极易溶于水.
解答 解:A.除杂时导管长进短出,则图中进气导管不合理,不能除杂,故A错误;
B.氯气的密度比空气的密度大,且氯气易与NaOH溶液反应,则烧瓶中氯气的进气导管过长,不利于气体的收集,若导管短易发生倒吸,故B错误;
C.氯气与浓硫酸不反应,浓硫酸具有吸水性,则浓硫酸可干燥氯气,且进气导管合理,故C正确;
D.HCl极易溶于水,导管在液面下,易发生倒吸,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验装置的分析、防倒吸装置、气体的干燥和收集等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
17.下列变化或事实与范德华力无关的是( )
| A. | 气体物质加压或降温时能凝结或凝固 | |
| B. | 碘溶于四氯化碳 | |
| C. | 氟、氯、溴、碘单质的熔沸点依次升高 | |
| D. | 食盐熔化 |
5.下列变化中,不需要破坏化学键的是( )
| A. | 加热碳酸氢钠 | B. | 氯化氢溶于水 | C. | 食盐熔化 | D. | 干冰气化 |
2.有关化学用语正确的是( )
| A. | 乙烯的实验式:C2H4 | B. | 乙炔的电子式: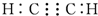 | ||
| C. | 乙醇的结构简式:C2H6O | D. | 氢氧根电子式: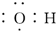 |
19.对于达到平衡状态的可逆反应:N2+3H2?2NH3,下列有关叙述正确的是( )
| A. | N2和NH3的质量分数相等 | B. | N2、H2、NH3的浓度之比为1:3:2 | ||
| C. | 反应物和生成物浓度不再发生变化 | D. | 正反应和逆反应不再进行 |
6.对于反应2SO2+O2$?_{加热}^{催化剂}$2SO3,下列判断正确的是( )
| A. | 2 mol SO2和足量的O2反应,可生成2 mol SO3 | |
| B. | 达到反应限度时SO2、O2、SO3的分子数之比一定为2:1:2 | |
| C. | 达到反应限度时SO2的消耗速率必定等于O2的生成速率的2倍 | |
| D. | 若反应在恒容容器中进行,气体密度保持不变,可以判定反应到达平衡 |
4.右图是元素周期表的一部分,关于图中阴影部分元素的说法中,正确的是( )
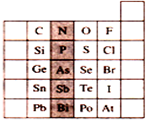

| A. | PH3的沸点比NH3高 | |
| B. | PH3的稳定性比H2S强 | |
| C. | 该纵行元素的最高价氧化物对应的水化物化学式均为H3RO4 | |
| D. | H3AsO4的酸性比H3PO4弱 |
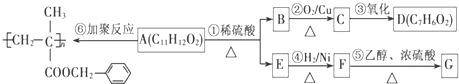
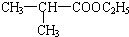 .
.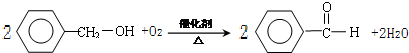 .
.