题目内容
(1)已知10g CaCO3分解需要吸收17.56kJ 热量,请写出碳酸钙分解的热化学反应方程式: 。
(2)加热5.00 g碳酸钠和碳酸氢钠的混合物,反应完成后混合物的质量减少了0.31 g,则原混合物中碳酸钠的质量为 g。
(4分)(1)CaCO3(s)=CaO(s) + CO2(g) ΔH=+175.6kJ·mol-1 (2)4.16
解析试题分析:(1)10g CaCO3分解需要吸收17.56kJ 热量,则1mol即100g碳酸钙分解需要消耗的能量是175.6kJ,因此该反应的热化学方程式是CaCO3(s)=CaO(s) + CO2(g) ΔH=+175.6kJ·mol-1。
(2)碳酸氢钠分解的方程式是2NaHCO3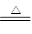 Na2CO3+H2O+CO2↑ △m↓
Na2CO3+H2O+CO2↑ △m↓
2×84g 106g 62g
m 0.31g
解得m=(62g×0.31g)÷168g=0.84g
所以原混合物中碳酸钠的质量为5.00g-0.84g=4.16g
考点:考查热化学方程式的书写、混合物的有关计算
点评:该题是基础性试题的考查,难度不大,有利于培养学生规范的答题能力,在计算碳酸钠的质量时,注意利用好差量法,注意有关解题方法的归纳和总结。

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
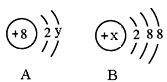
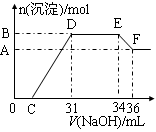
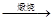 2Fe2O3+8SO2
2Fe2O3+8SO2