题目内容
有一硫酸和硝酸的混合溶液,取出20mL,加入足量BaCl2溶液,经过滤、洗涤、烘干后得沉淀9.32g;滤液与4.0mol/L的氢氧化钠溶液35mL恰好完全中和。试求:
(1)原混合溶液中硫酸和硝酸的物质的量浓度。
(2)另取10mL原溶液,加入0.96g铜粉共热,生成一氧化氮的体积为多少?
(3)另取10mL原溶液,加入1.92g铜粉共热,,至少还要向反应后的溶液中加入多少毫升1mol/L硫酸才能将铜粉恰好完全溶解?
(1)c(H2SO4)= 2mol/L c(HNO3)= 3mol/L
(2)标准状况下的体积V(NO)= 0.224L
(3)5×10-3L
解析试题分析:(1)20 mL混合液中含有n(SO42-)="9.32g÷233g/" mol="0.04" mol
n(H+)=35×10-3×4.0 mol / L ="0.14" mol
∴n((NO3-)="0.14" mol-2×0.04 mol =0.06mol
c(H2SO4)=0.04mol÷0.02L=2mol/L (1分)
c(HNO3)=0.06mol÷0.02L=3mol/L (1分)
(2) 10 mL混合液中含有n(H+)="0.07" mol,n(NO3-)=0.03mol
加入0.96g铜粉:n(Cu)=0.96g÷64g/mol=0.015mol
发生反应:3Cu + 8H++ 2NO3 - 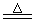 3Cu2+ + 2NO↑ + 4H2O
3Cu2+ + 2NO↑ + 4H2O
铜粉不足,生成NO:n(NO)=0.015mol×2÷3= 0.01 mol (1分)
标准状况下的体积V(NO)=" 0.01" mol×22.4 L / mol =0.224L (1分)
(3)10 mL混合液中含有n(H+)="0.07" mol,n((NO3-)=0.03mol
若加入1.92g铜粉:n(Cu)=1.92g÷64g/mol=0.03mol
发生反应:3Cu + 8H++ 2NO3 -  3Cu2+ + 2NO↑ + 4H2O
3Cu2+ + 2NO↑ + 4H2O
溶解1.92g铜粉至少需要n(H+)="0.08" mol ,n(NO3-)=0.02mol,显然H+不足(1分)
至少需要添加n(H+)="0.08" mol-0.07 mol="0.01" mol
∴ 至少加入稀硫酸:V(H2SO4)=0.01mol÷(2×1mol/L)=5×10-3L (2分)
答:略
考点:考查物质的量在化学反应方程式中的应用的相关知识点。

下表是用沉淀法测定KHCO3和Na2CO3混合物的组成的相关数据。实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,每次实验均充分反应。实验记录见下表:
| 实验次数 | 称取样品的 质量/g | 所加Ba(OH)2 溶液的体积/L | 测得生成沉淀 的质量/g |
| 1 | 0.518 | 0.5 | 0.985 |
| 2 | 1.036 | 0.5 | |
| 3 | 1.554 | 0.5 | 2.955 |
| 4 | 2.072 | 0.5 | 3.940 |
| 5 | 2.590 | 0.5 | 3.940 |
| 6 | 3.108 | 0.5 | 3.940 |
(1)第2次实验中产生沉淀多少克?请将结果填在表格相应空格中。
(2)样品中KHCO3和Na2CO3的物质的量之比是 。
(3)室温下,取上述Ba(OH)2溶液50 mL,加入0.05 mol·L-1的盐酸,反应后所得溶液的pH=2,求所加盐酸的体积(混合时不考虑溶液体积变化,写出计算过程)。
Na2O2曾经是潜水艇或航天器中最理想的供氧剂。下表是人体呼出气体的成分(均为体积百分含最)。
| | 空气 成分 | 人体呼出 气体成分 |
| N2 | 78% | 74% |
| O2 | 21% | 16% |
| H2O | 0. 5% | 6% |
| CO2 | 0. 03% | 4% |
(1)已知一个人一天大约要产生16 mol CO2。若全部被Na2O2吸收,需要Na2O2________ g。
(2)若要使被吸收的CO2与产生的O2体积相等,就需
要在Na2O2中添加KO2.计算要达到该目的.Na2O2与KO2的物质的量比例是 。
已知:4KO2+2CO2=2K2CO3+3O2
(3)计算100 L空气经过人体呼吸后,呼出气体中O2的体积(标准状况下,保留2位小数)____ L。
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处 理,无用物质排出航天器。100 L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100 L(可供使用的化学试剂只有Na2O2).通过计算回答:若先利用CO2,还需要利用水蒸气,求需要水蒸气体积 L。