题目内容
6.某学生用质量分数为98%、密度为1.84g•cm-3的浓硫酸,配制0.2moL•L-1的硫酸溶液500mL.试回答下列问题:(1)计算所需浓硫酸的体积5.4mL.
(2)从下列用品中选出实验所需要的仪器BCEI(填序号).
A.1000mL烧杯 B.100mL烧杯 C.10mL量筒
D.100mL量筒 E.500mL容量瓶.F.1000mL容量瓶
G.广口瓶 H.托盘天平 I.玻璃棒
除选用上述仪器外,尚缺少必要的仪器或用品是胶头滴管.
(3)该学生根据计算结果,进行如下实验操作:
①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;
③立即将稀释后的溶液转入容量瓶中;
④然后小心地用烧杯往容量瓶中加蒸馏水至刻度线;
⑤把容量瓶盖盖紧,再振荡摇匀.
指出上述实验中错误的操作是②③④(用编号表示).
分析 (1)先根据c=$\frac{1000ρω}{M}$计算出浓硫酸的物质的量浓度,然后根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
(2)根据配制一定物质的量浓度的溶液的实验操作步骤选择仪器,然后判断还缺少的仪器;
(3)①可以用量筒量取计算所需体积的浓硫酸;
②量筒不能用来稀释溶液;
③浓硫酸稀释后放热,应恢复至室温后再将将稀释后的溶液转入容量瓶中;
④蒸馏水至液面至刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低点与刻度线相切;
⑤把容量瓶盖盖紧,振荡摇匀.
解答 解:(1)浓硫酸的物质的量浓度为c=$\frac{1000ρω}{M}$mol/L=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
设所需浓硫酸的体积为V,则有V×18.4mol/L=O.5L×0.2mol/L,
则:V=$\frac{0.5L×0.2mol/L}{18.4nol/L}$=O.0054L=5.4mL,
故答案为:5.4mL;
(2)配制0.2mol/L的硫酸溶液500mL稀硫酸,操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,
所需要的仪器为:烧杯、筒量、玻璃棒、500mL容量瓶、胶头滴管,所以缺少的仪器为胶头滴管,
故答案为:BCEI;胶头滴管;
(3)①用量筒量取计算所需体积的浓硫酸,故①正确;
②量筒不能用来稀释溶液,故②错误;
③浓硫酸稀释后放热,应恢复至室温后再将将稀释后的溶液转入容量瓶中,故③错误;
④蒸馏水至液面至刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低点与刻度线相切,故④错误;
⑤定容后把容量瓶盖盖紧,然后振荡摇匀即可,故⑤正确;
故答案为:②③④.
点评 本题考查了配制一定物质的量浓度的溶液的方法,题目难度不大,明确配制一定物质的量浓度的步骤及误差分析方法为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
| A. | 电解过程中共转移电子1.4mol | |
| B. | 原硫酸铜溶液的体积为1L | |
| C. | 在这个过程中共生成6.4gCu和0.5molO2 | |
| D. | 电解过程中阴极有0.3molH2生成 |
| A. | 等于(a-0.8 )g | B. | 大于(a-0.8 )g | C. | 大于(a-2.67)g | D. | 等于(a-2.67)g |
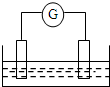 如图是常见原电池装置,电流表G发生偏转:
如图是常见原电池装置,电流表G发生偏转: 如图在试管甲中先加入2mL 95%的乙醇,再加入2克无水乙酸,充分摇匀,并在摇动下缓缓加入2mL浓硫酸,冷却后,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL 95%的乙醇,再加入2克无水乙酸,充分摇匀,并在摇动下缓缓加入2mL浓硫酸,冷却后,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: CH3COOC2H5+H2O
CH3COOC2H5+H2O E的元素符号是Cl.
E的元素符号是Cl.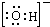 .
.