题目内容
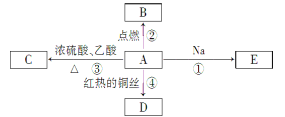
【题目】有机物 G(分子式为 C13H18O2)是一种香料,其合成路线如下图所示。
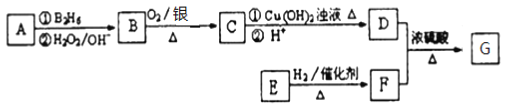
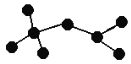
已知:(1) ![]()
(2) 有机物A属于烃类,其相对分子质量为56,核磁共振氢谱有2组峰
(3) E能发生银镜反应,1molE与2molH2可以发生反应生成F
(4)有机物F是苯甲醇的同系物,苯环上只有一个无支链的侧链
回答下面的问题:
(1)有机物B:____________,反应E→F的反应类型为:____________;
(2)E的结构简式为____________:
(3)A在一定条件下生成高分子化合物的化学方程式为____________;
(4)D+F→G 的化学方程式:____________;
(5)已知有机化合物甲符合下列条件:①芳香族化合物②与F互为同分异构体③能被催化氧化成醛。符合上述条件的有机物甲有____________种。其中满足苯环上有3个侧链,且核磁共振氢谱有5组峰的有机物的结构简式为(写出符合条件的其中一种即可)____________ 。
【答案】(1)2-甲基-1-丙醇 加成反应(或还原反应) (2)C6H5-CH=CHCHO
(3)![]()
(4)(CH3)2CHCOOH +C6H5-CH2CH2CH2OH![]() (CH3)2CHCOOCH2CH2CH2-C6H5 +H2O
(CH3)2CHCOOCH2CH2CH2-C6H5 +H2O
(5)13 种 
【解析】
试题分析:有机物A属于烃类,其相对分子质量为56,分子式为C4H8,核磁共振氢谱有2组峰,则A为CH3CH=CHCH3或(CH3)2C=CH2,A发生信息中的反应生成B,B可以连续发生氧化反应,A的核磁共振氢谱有2组峰,则A为(CH3)2C=CH2,B的结构简式为(CH3)2CHCH2OH,C的结构简式为(CH3)2CHCHO,有机物F是苯甲醇的同系物,苯环上只有一个无支链的侧链,结合G的分子式可知F的结构简式为:![]() ,则G为
,则G为![]() ,E能发生银镜反应,在一定条件下1molE能与2molH2反应生成F,则E为
,E能发生银镜反应,在一定条件下1molE能与2molH2反应生成F,则E为![]() ;
;
(1)B的结构简式为(CH3)2CHCH2OH,由![]() 生成
生成![]() 的反应类型为加成反应或还原反应;
的反应类型为加成反应或还原反应;
(2)E的结构简式为![]() :
:
(3)(CH3)2C=CH2在一定条件下生成高分子化合物的化学方程式为![]() ;
;
(4)D+F→G的化学方程式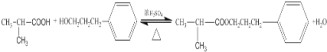 ;
;
(5)已知有机物甲符合下列条件:①为芳香族化合物,说明含有苯环;②与F(![]() )互为同分异构体;③能被催化氧化成醛,含有-CH2OH结构,含有一个取代基为-CH(CH3)CH2OH,含有2个取代基为-CH3、-CH2CH2OH或者-CH2CH3、-CH2OH,各有邻、间、对3种,含有3个取代基为2个-CH3和-CH2OH,2个-CH3处于邻位,-CH2OH有2种位置,2个-CH3处于间位,-CH2OH有3种位置,2个-CH3处于对位,-CH2OH有1种位置,符合上述条件的有机物甲有13种,其中一种苯环上有3个侧链,且核磁共振氢谱有5组峰的有机物的结构简式:
)互为同分异构体;③能被催化氧化成醛,含有-CH2OH结构,含有一个取代基为-CH(CH3)CH2OH,含有2个取代基为-CH3、-CH2CH2OH或者-CH2CH3、-CH2OH,各有邻、间、对3种,含有3个取代基为2个-CH3和-CH2OH,2个-CH3处于邻位,-CH2OH有2种位置,2个-CH3处于间位,-CH2OH有3种位置,2个-CH3处于对位,-CH2OH有1种位置,符合上述条件的有机物甲有13种,其中一种苯环上有3个侧链,且核磁共振氢谱有5组峰的有机物的结构简式:![]() 。
。