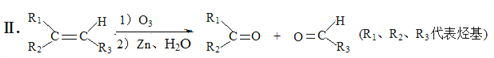
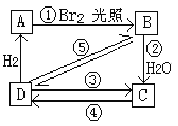
题目内容
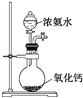
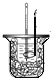
【题目】下图所示装置Ⅰ是可充电电池.已知:该充电电池充电时的反应为:Na2Sx+3NaBr→2Na2Sy+NaBr3,闭合开关K时, 装置Ⅱ中b极附近变红色。下列说法正确的是
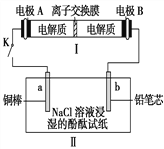
A. 闭合开关K时,电极B上发生的反应是:Br3- + 2e- =3Br-
B. 闭合开关K时,I中Na+移向A极,II中Na+移向a极
C. 当有0.01 mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112 mL
D. 闭合开关K时,Ⅱ中发生反应的离子方程式为:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
【答案】C
【解析】当闭合开关K时,b极附近溶液变红色,说明b极生成OH-离子,为电解池的阴极,发生反应为2H2O+2e-=H2↑+2OH-,则B为原电池的负极,A为原电池的正极,根据电池充电的化学反应方程式为Na2Sx+3NaBr→2Na2Sy+NaBr3可知,阴极反应为Na2Sx+2e-+2Na+=2Na2Sy,阳极反应为3NaBr-2e-=NaBr3+2Na+,a极为电解池的阳极,电极反应为2Cu-2e-=Cu2+。A. 闭合开关K时,电极B为负极,发生氧化反应, Br3- +2e- =3Br-为还原反应,故A错误;B. 闭合开关K时,原电池中阳离子有负极移向正极,I中Na+移向A极,电解池中,阳离子移向阴极,II中Na+移向b极,故B错误;C. 当有0.01 mol Na+通过离子交换膜时,转移0.01mol电子,b电极上析出0.005mol氢气,标准状况下的气体112 mL,故C正确;D. 闭合开关K时,Ⅱ中a极为电解池的阳极,电极反应为2Cu-2e-=Cu2+,故D错误;故选C。

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】下列实验装置或方案不能达到实验目的的是
编号 | A | B | C | D |
实验装置或 方案 |
|
|
50mL0.5mol/LHCl与50mL0.55mol/LNaOH溶液 |
|
目的 | 制备少量氨气 | 配制0.10mol/L NaOH溶液 | 测定中和热 | 探究Ksp(AgCl)与Ksp(AgI)的大小 |
A. A B. B C. C D. D