题目内容
【题目】下列实验装置或方案不能达到实验目的的是
编号 | A | B | C | D |
实验装置或 方案 |
|
|
50mL0.5mol/LHCl与50mL0.55mol/LNaOH溶液 |
|
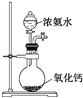
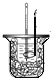
目的 | 制备少量氨气 | 配制0.10mol/L NaOH溶液 | 测定中和热 | 探究Ksp(AgCl)与Ksp(AgI)的大小 |
A. A B. B C. C D. D
【答案】B
【解析】A. 氧化钙与水反应放热,使浓氨水分解放出氨气,故A正确;B. 容量瓶不能用作溶解氢氧化钠固体的仪器,溶解应该在小烧杯中进行,故B错误;C. 测定中和热,用稍过量的氢氧化钠与盐酸反应,能够使盐酸完全反应,且装置图没有问题,故C正确;D. 在氯化钠溶液中滴加几滴硝酸银溶液生成白色沉淀,生成的氯化银存在溶解平衡,再加入几滴碘化钾溶液,生成溶解度更小的碘化银沉淀,说明Ksp(AgCl)>Ksp(AgI),故D正确;故选B。

练习册系列答案
相关题目