题目内容
5.过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.根据四个H2O2参与的化学方程式判断下列说法正确的是( )①Na2O2+2HCl=2NaCl+H2O2
②Ag2O+H2O2=2Ag+O2↑+H2O
③2H2O2=2H2O+O2↑
④3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O.
| A. | 上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是Ag2O>H2O2>K2CrO4 | |
| B. | H2O2既体现氧化性又体现还原性的反应是①③ | |
| C. | H2O2仅体现氧化性的反应是② | |
| D. | H2O2仅体现还原性的反应是③ |
分析 A.氧化还原反应中,氧化剂的氧化性>氧化产物的氧化性;
B.①中没有元素化合价的变化;
C.②中H2O2中O元素的化合价升高;
D.化合价升高,体现还原性.
解答 解:A.反应Ag2O+H2O2=2Ag+O2↑+H2O中,氧化银做氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,反应3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O中,双氧水做氧化剂,铬酸钾做氧化产物,则氧化性H2O2>K2CrO4,故氧化性顺序为:Ag2O>H2O2>K2CrO4,故A正确;
B.①Na2O2+2HCl=2NaCl+H2O2中没有元素化合价的变化,不属于氧化还原反应,故B错误;
C.②中H2O2中O元素的化合价升高,作还原剂,体现还原性,故C错误;
D.③2H2O2=2H2O+O2↑中O元素的化合价即升高又降低,既体现氧化性又体现还原性的反应,故D错误.
故选A.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重基本概念的考查,注意把握氧化性的比较方法,题目难度不大.

练习册系列答案
相关题目
16.化学与人类生活密切相关.下列说法正确的是( )
| A. | “钡餐”中使用的硫酸钡是弱电解质 | |
| B. | 镀锌铁镀层破损后,铁更容易被腐蚀 | |
| C. | 提倡人们购物时不用塑料袋,是为了防止白色污染 | |
| D. | 推广使用太阳能、风能、海洋能、氢能,不利于缓解温室效应 |
13.核电站遭破坏,会造成放射性物质I和Cs向外界泄漏.下列有关说法错误的是( )
| A. | 每个Cs含有82个中子 | B. | CsOH的碱性比KOH的强 | ||
| C. | HI的还原性比HF的强 | D. | KIO3是碘的最高价含氧酸的盐 |
10.下列有关σ键和π键的说法错误的是( )
| A. | 在某些分子中,化学键可能只有π键而没有σ键 | |
| B. | 当原子形成分子时,首先形成σ键,可能形成π键,配位键都是σ键 | |
| C. | σ键的特征是轴对称,π键的特征是镜面对称 | |
| D. | 含有π键的分子在反应时,π键是化学反应的积极参与者 |
20.常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ/mol).如表是一些键能数据:
(1)根据键能数据计算以下反应的反应热:CH4(g)+4F2(g)═CF4(g)+4HF(g);△H=-1928KJ/mol.
(2)根据键能和反应热化学方程式N2(g)+H2(g)═NH3(g);△H=-46KJ/mol,则N=N的键能为946kJ/mol.
| 化学键 | C-H | C-F | H-F | F-F | H-H | H-N |
| 键 能 | 414 | 489 | 565 | 158 | 436 | 391 |
(2)根据键能和反应热化学方程式N2(g)+H2(g)═NH3(g);△H=-46KJ/mol,则N=N的键能为946kJ/mol.

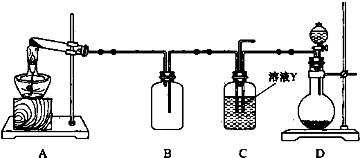
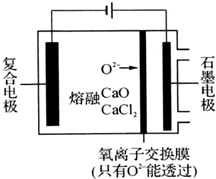 纳米二氧化钛作为一种新型的光催化剂,其用途相当广泛.金属钛具有优良的性能,是航天工业的重要材料.水解法制备纳米二氧化钛和电解钛的过程如下:
纳米二氧化钛作为一种新型的光催化剂,其用途相当广泛.金属钛具有优良的性能,是航天工业的重要材料.水解法制备纳米二氧化钛和电解钛的过程如下: