题目内容
8.下列有关甲烷的叙述不正确的是( )| A. | 甲烷是最简单的有机物 | |
| B. | 甲烷是天然气的主要成分 | |
| C. | 甲烷能与氯气在光照条件下发生反应 | |
| D. | 甲烷能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色 |
分析 甲烷为最简单的有机化合物,是天然气和沼气的主要成分,与氯气在光照条件下发生取代反应,性质较为稳定,不与强酸、强碱强氧化剂等反应,据此解答即可.
解答 解:A、甲烷为最简单的有机化合物,故A正确;
B、甲烷值天然气、沼气以及狂道坑气的主要成分,故B正确;
C、甲烷在光照下与氯气发生取代反应生成一氯甲烷、二氯甲烷等,故C正确;
D、性质较为稳定,不与强酸、强碱、强氧化剂等反应,即不能使高锰酸钾溶液褪色,故D错误,故选D.
点评 本题主要考查的是甲烷的结构以及性质和甲烷的存在形式,难度不大,掌握课本内容即可轻松解答.

练习册系列答案
相关题目
13.创建和谐社会,保护生存环境是每一个公民的责任和义务.下列做法不符合人与自然和谐相处的是( )
| A. | 对废旧电池进行回收处理 | |
| B. | 购物时尽量不用塑料袋 | |
| C. | 对聚乙烯等塑料垃圾进行深埋或倾倒入海 | |
| D. | 使用沼气、太阳能、风能等能源替代传统的煤炭 |
14.向下列物质中加入金属钠和碳酸钠都能产生气体的物质是( )
| A. | H2O | B. | CH3COOC2H5 | C. | CH3CH2OH | D. | CH3COOH |
16.当光束分别通过下列分散系时,能观察到丁达尔效应的是( )
| A. | NaOH溶液 | B. | Fe(OH)3胶体 | C. | C2H5OH溶液 | D. | CuSO4溶液 |
3.下列有关反应2NO+2CO$\frac{\underline{\;催化剂\;}}{△}$N2+CO2的叙述中,正确的是( )
| A. | 该反应是复分解反应 | B. | NO发生还原反应 | ||
| C. | CO是氧化剂 | D. | 反应物中O得电子 |
13.下列有关硫酸和硝酸的叙述正确的是( )
| A. | 在加热条件下,浓硫酸和浓硝酸均能与木炭反应 | |
| B. | 将浓硫酸和浓硝酸分别长期露置于空气中,浓度均会升高 | |
| C. | 稀硫酸和稀硝酸分别与金属反应时,S和N元素的化合价都会发生变化 | |
| D. | 因为浓硫酸和浓硝酸都能与铝反应,所以常温下二者都不能用铝制容器盛放 |
20.下列反应中,属于加成反应的是( )
| A. | 乙醇与金属钠反应 | B. | 苯和液溴反应生成溴苯 | ||
| C. | 乙烯和溴的四氯化碳溶液反应 | D. | 乙酸和乙醇反应生成乙酸乙酯 |
17.某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4•7H2O)产品,设计流程如下:

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.
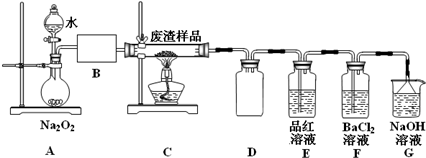
①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).
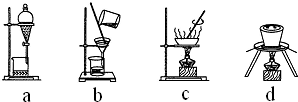
步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是ad(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.

①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).

步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.90 | 20.02 | 19.98 | 20.00 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.
18.25℃时,0.1mol•L-1氨水中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-8,下列叙述正确的是( )
| A. | 该溶液中氢离子的浓度:c(H+)=1×10-11mol•L | |
| B. | pH=7的NH4Cl和NH3•H2O的混合溶液:c(Cl-)>c(NH4+)>c(H+)>c(H+)=c(OH-) | |
| C. | 浓度均为0.1mol•L-1的NH3•H2O和NH4Cl溶液等体积混合后的碱性溶液中:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) | |
| D. | 0.1mol•L-1的氨水与0.05mol的H2SO4溶液等体积混合后所得溶液中:2c(NH4+)+2c(NH3•H2O)=c(SO42-) |