题目内容
【题目】工业以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:

(1)浸锰过程中Fe2O3与SO2反应的离子方程式为Fe2O3+ SO2+2H+=2Fe2++ SO42-+ H2O,该反应是经历以下两步反应实现的。
ⅰ:Fe2O3 + 6H+ = 2Fe3++3H2O ⅱ: ......
写出ⅱ的离子方程式:____________________________________________。
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为_______(填离子符号)。
(3)氧化过程中被MnO2氧化的物质有(写化学式):____________________。
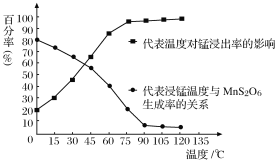
(4)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是_________;向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度不宜太高的原因是______________________。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:_____________________。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_________________________________。
【答案】2Fe3++ SO2+2H2O= 2Fe2+ + SO42-+4H+ Mn2+ Fe2+ SO2(H2SO3)、 FeSO4 90℃ 防止NH4HCO3受热分解,提高原料利用率 Mn2++2HCO3-=MnCO3↓+CO2↑+H2O 取1-2mL最后一次洗液于试管,滴加盐酸酸化BaCl2溶液,若无白沉淀产生,则洗涤干净
【解析】
分析一下工业流程:浸锰过程通入过量的SO2,将Mn4+和Fe3+还原成Mn2+和Fe2+,过滤Ⅰ所得滤渣为SiO2,加入MnO2氧化,此时溶液中可以被氧化的物质有Fe2+和未反应的SO2,调PH是为了将上一步氧化生成的Fe3+沉淀下来与Mn2+分离,加入NH4HCO3溶液将Mn2+沉淀下来,再经过一系列步骤可得到纯的MnCO3。
(1)用总反应离子方程式减去反应ⅰ可得反应ⅱ2Fe3++ SO2+2H2O= 2Fe2+ + SO42-+4H+ ;
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为上一步SO2将Mn4+和Fe3+还原成Mn2+和Fe2+,所以答案为Mn2+ 、 Fe2+;
(3)氧化过程中溶液中具有还原性的物质有Fe2+和未反应的SO2,被MnO2氧化的物质有SO2(H2SO3)、 FeSO4;
(4)从图像中可以看出,随着温度的升高,副产物MnS2O6生成率越来越低,当温度到达90℃,生成率基本不变,再升高温度意义不大,并且耗能,故“浸锰”的适宜温度是90℃,NH4HCO3溶液时在一定温度下会分解成NH3和CO2,向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度不宜太高的原因是防止NH4HCO3受热分解,提高原料利用率;
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,可判断出气体为CO2,不可能为NH3,应为如果生成NH3,则得不到MnCO3沉淀,反应的离子方程式:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;
(6)检验洗涤是否完全,需要检验最后一次洗涤液是否存在溶液中的粒子,这里选择SO42-,检验试剂选择BaCl2溶液,故方法为取1-2mL最后一次洗液于试管,滴加盐酸酸化BaCl2溶液,若无白沉淀产生,则洗涤干净。

【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=_________。
【题目】金属加工前常用盐酸对金属表面氧化物进行清洗,会产生酸洗废水。pH在2左右的某酸性废水含铁元素质量分数约3%,其他金属元素如铜、镍、锌浓度较低,综合利用酸洗废水可制备三氯化铁。制备过程如下:
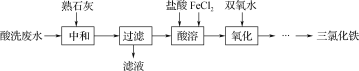
相关金属离子生成氢氧化物沉淀的pH如下表:
Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 | |
开始沉淀的pH | 1.5 | 4.2 | 7.1 | 5.4 |
沉淀完全的pH | 3.7 | 6.7 | 9.2 | 8.0 |
回答下列问题:
(1)“中和”时调节pH至________,有利于后续制备得纯度较高的产品。
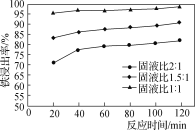
(2)处理酸洗废水中和后的滤渣,使铁元素浸出。按照不同的固液比投入“过滤”后滤渣和工业盐酸进行反应的铁浸出率如图所示,实际生产中固液比选择1.5∶1的原因是__________________。
(3)写出“氧化”中发生反应的离子方程式:____________________________________。
(4)“酸溶”后需根据溶液中Fe2+含量确定氧化剂的投入量。用K2Cr2O7标准溶液测定Fe2+(Cr2O![]() 被还原为Cr3+)的含量,该反应离子方程式为____________________________。
被还原为Cr3+)的含量,该反应离子方程式为____________________________。
(5) 将三氯化铁溶液在一定条件下________、________、过滤、洗涤、在氯化氢气氛中干燥得FeCl3·6H2O晶体,在实验室过滤装置中洗涤固体的方法是___________________。