题目内容
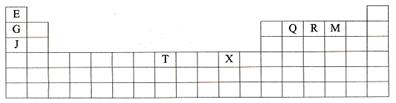
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)B、D、F、G的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)请写出元素H的基态原子电子排布式_____________________。
(3)A的最简单氢化物分子里中心原子采取________形式杂化,A的最高价氧化物分子的空间构型是________。
(4)D的氯化物的熔点比G的氯化物的熔点________(填“高”或“低”),理由是__________________________。
(5)元素C与元素G形成的晶体所属的晶体类型为________晶体,在该晶体中原子间形成的共价键属于________(从下列选项中选出正确类型)。
A.σ键 B.π键 C.既有σ键,又有π键
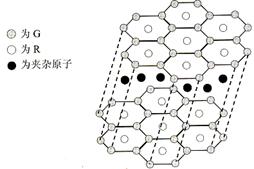
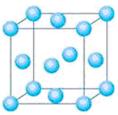
(6)F单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。晶胞中F原子的配位数为________,一个晶胞中F原子的数目为________。

试回答下列问题:
(1)B、D、F、G的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)请写出元素H的基态原子电子排布式_____________________。
(3)A的最简单氢化物分子里中心原子采取________形式杂化,A的最高价氧化物分子的空间构型是________。
(4)D的氯化物的熔点比G的氯化物的熔点________(填“高”或“低”),理由是__________________________。
(5)元素C与元素G形成的晶体所属的晶体类型为________晶体,在该晶体中原子间形成的共价键属于________(从下列选项中选出正确类型)。
A.σ键 B.π键 C.既有σ键,又有π键
(6)F单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。晶胞中F原子的配位数为________,一个晶胞中F原子的数目为________。

(共11分) (1)Na<Al<Si<N(1分)
(2)1s22s22p63s23p63d54s2(或[Ar]3d54s2)(1分)
(3)sp3(1分) 直线形(1分)
(4)高 (1分)NaCl为离子晶体,而SiCl4为分子晶体(2分)
(5)原子(1分) A (1分) (6)12(1分) 4(1分)
(2)1s22s22p63s23p63d54s2(或[Ar]3d54s2)(1分)
(3)sp3(1分) 直线形(1分)
(4)高 (1分)NaCl为离子晶体,而SiCl4为分子晶体(2分)
(5)原子(1分) A (1分) (6)12(1分) 4(1分)
(1)非金属性越强,第一电离能越大。所以大小顺序是Na<Al<Si<N。
(2)H是锰元素,根据构造原理可知,基态原子电子排布式为1s22s22p63s23p63d54s2(或[Ar]3d54s2)。
(3)碳的最简单氢化物是甲烷,由于碳原子中没有孤对电子,所以是正四面体形结构,采用sp3杂化。碳的最高价氧化物是CO2,属于直线型结构。
(4)钠的氯化物是氯化钠,形成的晶体是离子晶体,熔点高。硅的氯化物是四氯化碳,形成的晶体是分子晶体,熔点低。
(5)硅和氧形成的氧化物是二氧化硅,形成的晶体是原子晶体。硅原子和氧原子全部以单键相连,所以是σ键,答案选A。
(6)F是Al,根据晶胞的结构可知,配位数是3×8÷2=12。含有的原子数是8×1/8+6×1/2=4。
(2)H是锰元素,根据构造原理可知,基态原子电子排布式为1s22s22p63s23p63d54s2(或[Ar]3d54s2)。
(3)碳的最简单氢化物是甲烷,由于碳原子中没有孤对电子,所以是正四面体形结构,采用sp3杂化。碳的最高价氧化物是CO2,属于直线型结构。
(4)钠的氯化物是氯化钠,形成的晶体是离子晶体,熔点高。硅的氯化物是四氯化碳,形成的晶体是分子晶体,熔点低。
(5)硅和氧形成的氧化物是二氧化硅,形成的晶体是原子晶体。硅原子和氧原子全部以单键相连,所以是σ键,答案选A。
(6)F是Al,根据晶胞的结构可知,配位数是3×8÷2=12。含有的原子数是8×1/8+6×1/2=4。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目



 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。