题目内容
【题目】利用图示装置进行实验,反应进行足够长时间后装置II中实验现象正确的是
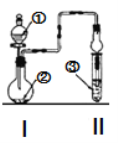
① | ② | ③ | II中实验现象 | |
A | 浓盐酸 | 大理石 | 氯化钡溶液 | 产生大量白色沉淀 |
B | 浓氨水 | 碱石灰 | 硫酸亚铁溶液 | 产生大量白色沉淀 |
C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 |
D | 浓盐酸 | KMnO4 | 氢硫酸 | 产生淡黄色沉淀 |
A.AB.BC.CD.D
【答案】D
【解析】
A.反应生成二氧化碳气体,且盐酸易挥发,二氧化碳与氯化钡溶液不反应,观察到Ⅱ中溶液无明显变化,不能产生白色沉淀,选项A错误;
B.反应生成氨气,氨气与硫酸亚铁溶液反应生成白色沉淀氢氧化亚铁,氢氧化亚铁被氧气,沉淀变为灰绿色,最后变为红褐色,则观察到Ⅱ中先生成白色沉淀,沉淀变为灰绿色,最后变为红褐色,后选项B错误;
C.酯化反应需要加热,则图中装置不能生成乙酸乙酯,选项C错误;
D.反应生成氯气,氯气与氢硫酸反应生成盐酸的硫沉淀,则观察到Ⅱ中出现淡黄色沉淀,选项D正确;
答案选D。

练习册系列答案
相关题目