题目内容
【题目】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
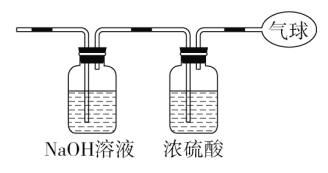
(1)如图是自来水表的常见安装方式,发生腐蚀过程中,电流从___(填“接头流向水表”或“水表流向接头”)。

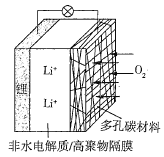
(2)某二次电池放电的电池反应为2Fe+O2+2H2O=2Fe(OH)2。反应结束时,电池的负极的质量___(“减小”“不变”或“增加”),该电池的正极反应式为___。
(3)有如图装置:
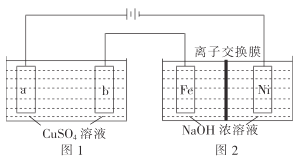
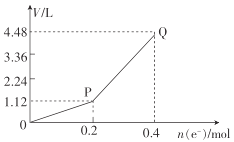
①图1中,用惰性电极电解过程中的实验数据如图,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中图1装置中产生气体的总体积(标准状况)。电解过程中转移n(e-)=0.4mol,b电极的实验现象为___;Q点时,a电极收集到的气体体积为___。
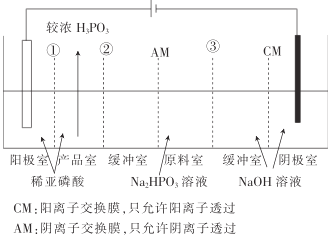
②图2中,装置通电后,溶液仍然保持澄清,铁电极附近呈紫红色(已知FeO42-在水溶液中呈紫红色),Fe电极上发生的电极反应式为___。
【答案】水表流向接头 增加 O2+4e-+2H2O=4OH- 先有红色物质析出,后有气泡产生 2.24L Fe-6e-+8OH-=FeO42-+4H2O
【解析】
(1)铁、铜、水溶液构成原电池,铁较活泼,失去电子,作负极,Cu作正极,电流方向由正极流向负极;
(3)①根据图示,同样是转移0.2mol电子,生成的气体体积不同,说明电极反应不同,开始是电解CuSO4和水,之后只有电解水。
(1)铁、铜、水溶液构成原电池,铁较活泼,失去电子,作负极,Cu作正极,电流方向由正极流向负极,电流方向为;水表流向接头;
(2)根据电池反应的,Fe失去电子化合价升高,作负极,转化为Fe(OH)2,则负极的质量增加;根据电池反应的产物Fe(OH)2,说明电解质溶液是中性或者碱性,O2在正极得到电子,与反应生成OH-,电极方程式为O2+4e-+2H2O=4OH-;
(3)①根据图示,OP阶段转移0.2mol电子,生成1.12L气体,而PQ阶段,转移0.2mol电子,生成3.36L气体,转移相同的电子,但是气体体积不同,说明两个阶段的电极反应不同。OP段,与电源正极相连的a电极,溶液中的OH-放电,电极方程式为2H2O-4e-=O2↑+4H+,转移了0.2mol电子,收集到1.12LO2;阴极,Cu2+放电,Cu2++2e-=Cu。PQ段,a电极上,依然是OH-放电,而b电极上,是H+放电,电极方程式为2H++2e-=H2↑,同样转移0.2mol电子,a电极上生成1.12LO2,而b电极上生成2.24LH2。电解过程中转移n(e-)=0.4mol,b电极上开始有铜生成,后有气体生成,实验现象为先有红色物质析出,后有气泡产生;a电极上总产生O2的体积为2.24L;
②图2中,装置通电后,溶液仍然保持澄清,铁电极生成FeO42-,Fe电极上发生的电极反应式为Fe-6e-+8OH-=FeO42-+4H2O。