题目内容
【题目】亚磷酸钠(Na2HPO3)溶液电渗析法制备H3PO3(亚磷酸)的原理如图所示,下列有关说法不正确的是( )
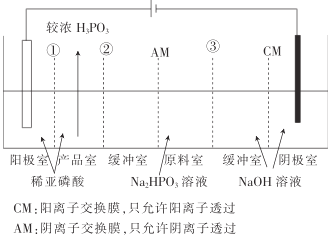
A.膜①、②、③均为CM
B.阴极的电极反应式为2H2O+2e-=2OH-+H2↑
C.阳极的电极反应式为2H2O-4e-=4H++O2↑
D.在原料室与产品室间设计缓冲室的主要目的是提高产品的纯度
【答案】A
【解析】
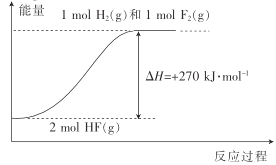
利用电解池制备H3PO3和NaOH,原料室中加入Na2HPO3,在电解池中阳离子向阴极移动,则Na+向右侧移动到达阴极室,在阴极,H+放电,电极方程式为2H2O+2e-=H2↑+2OH-,生成NaOH。HPO32-向阳极移动,到达产品室,在阳极,OH-放电,电极方程式为4H2O-4e-=O2↑+4H+,生成的H+向右侧移动,到达产品室,与HPO32-结合生成H3PO3,则①为CM,②为AM。
A.根据分析HPO32-向阳极移动,到达产品室。在阳极,OH-放电,电极方程式为4H2O-4e-=O2↑+4H+,生成的H+向右侧移动,到达产品室,与HPO32-结合生成H3PO3,则①为CM,②为AM,错误,A符合题意;
B.在阴极,H+放电,电极方程式为2H2O+2e-=H2↑+2OH-,正确,B不符合题意;
C.在阳极,OH-放电,电极方程式为4H2O-4e-=O2↑+4H+,正确,C不符合题意;
D.在产品室和原料室之间,设计缓冲室,可以减少杂质离子达到产品室,可以提高产品纯度,正确,D不符合题意。
答案选A。

练习册系列答案
相关题目