题目内容
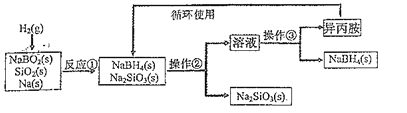
【题目】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
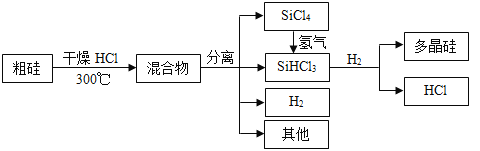
回答下列问题:
Ⅰ.硅粉与![]() 在300℃时反应生成
在300℃时反应生成![]() 气体和
气体和![]() ,放出
,放出![]() 热量,该反应的热化学方程式为________________________。
热量,该反应的热化学方程式为________________________。![]() 的电子式为__________________。
的电子式为__________________。
Ⅱ.将![]() 氢化为
氢化为![]() 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①![]()
![]()
②![]()
![]()
③![]()
![]()
(1)氢化过程中所需的高纯度![]() 可用惰性电极电解
可用惰性电极电解![]() 溶液制备,写出产生
溶液制备,写出产生![]() 的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。
的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。
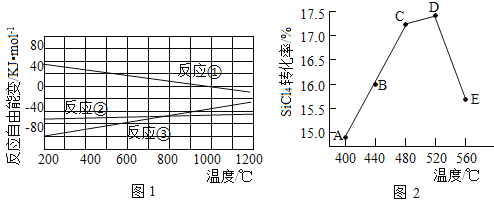
(2)已知体系自由能变![]() ,
,![]() 时反应自发进行。三个氢化反应的
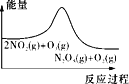
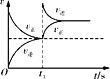
时反应自发进行。三个氢化反应的![]() 与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的
与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的![]() 小,主要原因是________________________。
小,主要原因是________________________。
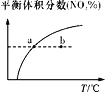
(3)不同温度下反应②中![]() 转化率如图2所示。下列叙述正确的是______(填序号)。
转化率如图2所示。下列叙述正确的是______(填序号)。
a.B点: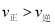 b.
b.![]() :A点
:A点![]() 点 c.反应适宜温度:
点 c.反应适宜温度:![]() ℃
℃
(4)反应③的![]() ______(用
______(用![]() ,
,![]() 表示)。温度升高,反应③的平衡常数
表示)。温度升高,反应③的平衡常数![]() ______(填“增大”、“减小”或“不变”)。
______(填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除![]() 、
、![]() 和
和![]() 外,还有______(填分子式)。
外,还有______(填分子式)。
【答案】
![]()
 阴极
阴极 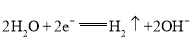 或
或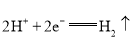 1000℃
1000℃ ![]() 导致反应②的
导致反应②的![]() 小 a、c
小 a、c ![]() 减小
减小 ![]() 、
、![]()
【解析】
I.书写热化学方程式时一定要标注出各物质的状态,要将热化学方程式中焓变的数值与化学计量数对应。本题的反应温度需要标注为条件;
II.(1)惰性电极电解KOH溶液,实质是电解水,产生氢气的必为阴极,发生还原反应。
(2)“看图说话”,将反应①的纵、横坐标对应起来看,即可顺利找到最低温度。影响自由能变的因素主要是焓变和熵变,分析发现熵变对反应②反而不利,说明焓变影响大,为主要影响因素;
(3)据图判断化学平衡的建立和移动是分析的关键。注意时间是一个不变的量。
(4)此问是盖斯定律的简单应用,对热化学方程式直接进行加减即可。
I.参加反应的物质是固态的Si、气态的HCl,生成的是气态的SiHCl3和氢气,反应条件是300℃,配平后发现SiHCl3的化学计量数恰好是1,由此可顺利写出该条件下的热化学方程式:Si(s)+3HCl(g) ![]() SiHCl3(g)+H2(g) H=-225kJ·mol-1;SiHCl3中硅与1个H、3个Cl分别形成共价单键,由此可写出其电子式为:
SiHCl3(g)+H2(g) H=-225kJ·mol-1;SiHCl3中硅与1个H、3个Cl分别形成共价单键,由此可写出其电子式为:![]() ,注意别漏标3个氯原子的孤电子对;
,注意别漏标3个氯原子的孤电子对;
II.(1)电解KOH溶液,阳极发生氧化反应而产生O2、阴极发生还原反应才产生H2;阴极的电极反应式可以直接写成2H++2e-=H2↑,或写成由水得电子也可以:2H2O+2e-=H2↑+2OH-;
(2)由题目所给的图1可以看出,反应①(最上面那条线)当G=0时,对应的横坐标温度是1000℃;从反应前后气体分子数的变化来看,反应①的熵变化不大,而反应②中熵是减小的,可见熵变对反应②的自发更不利,而结果反应②的G更负,说明显然是焓变产生了较大的影响,即H2<H1导致反应②的G小(两个反应对应的H,一个为正值,一个为负值,大小比较很明显);
(3)图2给的是不同温度下的转化率,注意依据控制变量法思想,此时所用的时间一定是相同的,所以图示中A、B、C点反应均正向进行,D点刚好达到平衡,D点到E点才涉及平衡的移动。在到达平衡状态以前,正反应速率大于逆反应速率,a项正确,B点反应正向进行,正反应速率大于逆反应速率;b点错误,温度越高,反应速率越快,所以E点的正(或逆)反应速率均大于A点;c项正确,C到D点,SiHCl3的转化率较高,选择此温度范围比较合适,在实际工业生产中还要综合考虑催化剂的活性温度。
(4)将反应①反向,并与反应②直接相加可得反应③,所以H3=H2-H1,因H2<0、H1>0,所以H3必小于0,即反应③正反应为放热反应,而放热反应的化学平衡常数随着温度的升高而减小;
(5)反应①生成的HCl可用于流程中粗硅提纯的第1步,三个可逆反应中剩余的H2也可循环使用。

 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/molS(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(1)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式_______________________________。
(2)在500℃下合成甲醇的反应原理为:
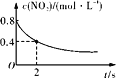
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g);在1L的密闭容器中,充入1mol CO2和3mol H2,压强为p0 kpa,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g);在1L的密闭容器中,充入1mol CO2和3mol H2,压强为p0 kpa,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)

①0~4min,H2的平均反应速率v(H2)=________mol·L1·min1。
②CO2平衡时的体积分数为______________,该温度下Kp为_________kPa-2_(用含有p0的式子表示,小数点后保留1位)。
③下列能说明该反应已达到平衡状态的是______________。
A.v正(CH3OH)=3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1∶3∶1∶1
C.恒温恒压下,气体的体积不再变化
D.恒温恒容下,气体的密度不再变化
④500℃、在2个容积都是2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 容器甲 | 容器乙 |
反应物起始投入量 | 1mol CO2,3mol H2 | 0.5mol CO2,1mol H2 1mol CH3OH,1mol H2O |
CH3OH的平衡浓度/mol·L1 | C1 | C2 |
则乙容器中反应起始向________(填“正反应”或“逆反应”)方向进行;c1_________(填“>”“<”或“=”)c2。