题目内容
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 水电离的c( H+)=1×l0-13 mol/L的溶液中:K+、Na+、SiO32-、SO42- | |
| B. | 能使石蕊呈蓝色的溶液中:Na+、Fe3+、SO42-、Cl- | |
| C. | $\frac{{K}_{W}}{c(O{H}^{-})}$=l×l0-13mol/L的溶液中:Ba2+、ClO-、Cl-、NO3- | |
| D. | 能与铝反应放出H2的溶液中:Fe2+、K+、SO42-、Cl- |
分析 A.水电离的c( H+)=1×l0-13 mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
B.能使石蕊呈蓝色的溶液呈碱性;
C.$\frac{{K}_{W}}{c(O{H}^{-})}$=l×l0-13mol/L的溶液呈碱性;
D.能与铝反应放出H2的溶液,可能为强碱性或非氧化性酸溶液.
解答 解:A.水电离的c( H+)=1×l0-13 mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下SiO32-不能大量共存,故A错误;
B.能使石蕊呈蓝色的溶液呈碱性,碱性条件下Fe3+不能大量共存,故B错误;
C.$\frac{{K}_{W}}{c(O{H}^{-})}$=l×l0-13mol/L的溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故C正确;
D.能与铝反应放出H2的溶液,可能为强碱性或非氧化性酸溶液,碱性条件下Fe2+不能大量共存,故D错误.
故选C.
点评 本题考查离子共存问题,为高考常见题型,题目难度中等,本题注意把握相关题给信息,为解答该类题目的关键,学习中注重相关基础知识的积累.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
17.在元素周期表的第四周期的主族元素中,金属元素的种数是( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
18.研究人员研制利用软锰矿浆(主要成分是MnO2)吸收流酸厂的尾气SO2,制备流酸锰的生产流程如下:
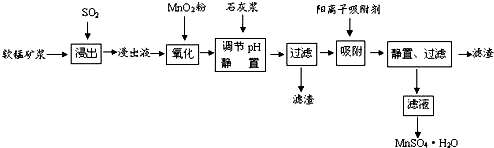
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+,等 其他金属离子,PbO2的氧化性大于MnO2,PbSO4是一种微溶物质.有关金属离子的半径、形成 氢氧化物沉淀时的pH见如表,阳离子吸附剂吸附金属离子的效果见如图.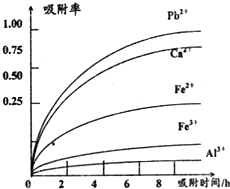
请回答下列问题:
(1)写出浸出过程中生成反应的化学方程式SO2+MnO2=MnSO4.
(2)氧化过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH值,此处调节pH值用到的仪器是pH计,应调节pH的范围为4.7≤pH<8.3.
(4)阳离子吸附剂可用于除去杂质金属离子•请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子的半径、金属离子的电荷等;吸附步骤除去的主要离子为:Pb2+、Ca2+.
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6.现将c mol•L-1CaCl2溶液与2.00×10-2
mol•L-1Na2SO4溶液等体积混合 (忽略体积的变化),则生成沉淀时,c的最小值是1.82×10-3mol•L-1.

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+,等 其他金属离子,PbO2的氧化性大于MnO2,PbSO4是一种微溶物质.有关金属离子的半径、形成 氢氧化物沉淀时的pH见如表,阳离子吸附剂吸附金属离子的效果见如图.

| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
(1)写出浸出过程中生成反应的化学方程式SO2+MnO2=MnSO4.
(2)氧化过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH值,此处调节pH值用到的仪器是pH计,应调节pH的范围为4.7≤pH<8.3.
(4)阳离子吸附剂可用于除去杂质金属离子•请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子的半径、金属离子的电荷等;吸附步骤除去的主要离子为:Pb2+、Ca2+.
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6.现将c mol•L-1CaCl2溶液与2.00×10-2
mol•L-1Na2SO4溶液等体积混合 (忽略体积的变化),则生成沉淀时,c的最小值是1.82×10-3mol•L-1.
2.甲基、苯基、羟基、羧基四种原子团中,不同的原子团两两结合,得到的物质中具有酸性的有( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 2种 |
12.除去如表各组物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 在空气中灼烧 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | H2O | 通过浓硫酸洗气 |
| A. | A | B. | B | C. | C | D. | D |
19.0.1mol两种气态烃组成的混合气体完全燃烧,得到0.16mol CO2和3.6g水.下列说法不正确的是( )
| A. | 混合气体中一定有甲烷 | B. | 混合气体中一定是甲烷和乙烯 | ||
| C. | 混合气体中一定没有乙烷 | D. | 混合气体中一定有乙炔 |
16.下列离方程式书写正确的是( )
| A. | 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| B. | NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+SO32-+2H2O | |
| C. | MnO2与浓盐酸制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| D. | AlCl3溶液中加入过量的氨水:Al3++4NH3•H2O=AlO2-+4NH4+ |
17.有机化学与生活密切相关,下列有关说法不正确的是( )
| A. | 苯酚不慎粘在皮肤上可用酒精洗涤 | |
| B. | 福尔马林是混合物 | |
| C. | 工业酒精只能作实验室燃料 | |
| D. | 服用豆浆或鸡蛋清可以缓解铜离子中毒 |