题目内容
18.下列关于铁的叙述正确的是( )①铁能被磁铁吸引,但纯铁比含杂质的铁易被腐蚀
②在人体的血红蛋白中含有铁元素
③铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
④铁与强氧化剂硝酸反应的产物只有一种是Fe(NO3)3
⑤不能通过化合反应制得FeCl2和Fe(OH)3.
| A. | ①③ | B. | ②③ | C. | ②⑤ | D. | ④⑤ |
分析 ①纯铁不易腐蚀;
②人体的血红蛋白中含有铁元素;
③铁与水蒸气反应生成四氧化三铁和氢气;
④铁过量,可生成Fe(NO3)2;
⑤氯化铁与铁化合生成氯化亚铁,氢氧化亚铁与氧气、水化合生成氢氧化铁.
解答 解:①铁合金易发生电化学腐蚀,纯铁不易腐蚀,故错误;
②人体的血红蛋白中含有铁元素,故正确;
③铁与水蒸气反应生成四氧化三铁和氢气,但不是燃烧,故正确;
④铁与硝酸反应,硝酸过量生成硝酸铁,铁过量生成硝酸亚铁,故错误;
⑤氯化铁与铁化合生成氯化亚铁,氢氧化亚铁与氧气、水化合生成氢氧化铁,二者都可以通过化合反应制取,故错误;
故选:B.
点评 本题综合考查铁及其化合物的性质,侧重于学生的分析能力和基础知识的综合运用,熟悉铁及其化合物性质是解题关键,题目难度不大.

练习册系列答案
相关题目
9.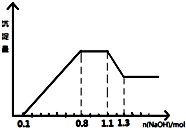 某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
 某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A. | 溶液中的阳离子只有H+、Mg2+、Al3+可能含有Fe3+ | |
| B. | 溶液中一定不含CO32-和NO3-,一定含有SO42- | |
| C. | 溶液中c(NH4+)=0.3 mol/L | |
| D. | c(H+):c(Al3+):c(Mg2+)=1:1:1 |
6.用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得的溶液中加入0.1mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解).则电解过程中转移电子的物质的量为( )
| A. | 0.4 mol | B. | 0.5 mol | C. | 0.6 mol | D. | 0.8 mol |
13.下列说法中,正确的是( )
| A. | 在化学反应过程中,发生物质变化的同时不一定发生能量变化 | |
| B. | 破坏生成物全部化学键所需要的能量小于破坏反应物全部化学键所需要的能量时,反应为放热反应 | |
| C. | 反应产物的总焓大于反应物的总焓时,即△H>0,反应吸热 | |
| D. | △H的大小与热化学方程式的化学计量数无关 |
3.某同学实验需要450mL0.1mol•L-1碳酸钠溶液,配制该溶液时下列仪器不需要的是( )
| A. | 100mL量筒、烧杯、玻璃棒 | B. | 托盘天平、500mL容量瓶 | ||
| C. | 酒精灯、三角漏斗、导管 | D. | 胶头滴管、玻璃棒、烧杯 |
7.一种气态烷烃和一种气态烯烃的混合物共10g,标况下的密度为1.116g/L.使混合气通过足量溴水,溴水增重8.4g,则混合气中的烃分别是( )
| A. | 甲烷和乙烯 | B. | 甲烷和丙烯 | C. | 乙烷和乙烯 | D. | 乙烷和丙烯 |
8.完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
| A. | 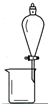 用CCl4提取溴水中的Br2 用CCl4提取溴水中的Br2 | B. |  从KI和I2的固体混合物中回收I2 从KI和I2的固体混合物中回收I2 | ||
| C. | 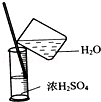 稀释浓硫酸 稀释浓硫酸 | D. | 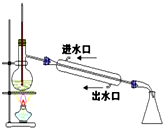 工业酒精制备无水酒精 工业酒精制备无水酒精 |