题目内容
15.如表是稀硫酸与某金属反应的实验数据:| 实验序号 | 金属 质量/g | 金属状态 | c(H2SO4) /mol•L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
(1)实验4和5表明,固体反应物的表面积对反应速率有影响,能表明同一规律的实验还有1和2(填实验序号);
(2)本实验中影响反应速率的除了浓度还有反应温度,仅表明该因素对反应速率产生影响的实验有6和7(填实验序号).
(3)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:因为所有反应中,金属质量和硫酸溶液体积均相等,且硫酸过量,产生热量相等,故溶液温度变化值相近.
分析 影响化学反应速率的因素有浓度、温度、催化剂以及固体表面积等,
固体颗粒的大小,在其他条件相同时,固体颗粒越小,反应物的表面积越大,化学反应速率越快;固体颗粒越小,固体反应物的表面积越小,化学反应速率降低;
反应物的浓度,在其他条件相同时,增大反应物的浓度,化学反应速率加快;减小反应物的浓度,反应速率降低;
反应物的温度,在其他条件相同时,升高反应物的温度,化学反应速率加快;降低反应物的温度,反应速率降低.
(1)实验1和2以及4和5固体的表面积不相同,硫酸浓度相同,可用于比较表面积对反应速率的影响;
(2)由表中数据可知,固体的表面积和硫酸的浓度以及温度影响反应速率;
(3)金属质量相等,完全反应放出的热量相同,则温度升高数值相等.
解答 解:(1)观察实验4和5,金属和稀硫酸的量相同,金属的状态不同,可知固体的表面积越大反应速率越快,能表明同一规律的实验还有1和2,
故答案为:固体反应物的表面积;1和2;
(2)本实验中,反应温度也影响化学反应速率,如实验6和7;
故答案为:反应温度;6和7;
(3)金属质量相等,如完全反应,放出的热量相同,因硫酸溶液体积均相等,且硫酸过量,则温度升高数值相等,溶液温度变化值相近,
故答案为:因为所有反应中,金属质量和硫酸溶液体积均相等,且硫酸过量,产生热量相等,故溶液温度变化值相近.
点评 本题考查影响化学反应速率的因素的探究,侧重于学生的分析能力和实验能力的考查,为高频考点,注意对比表中数据,把握影响反应速率的因素,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.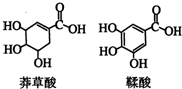 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸都能与溴水反应 | |
| B. | 两种酸遇三氯化铁溶液都显色 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 等物质的量的两种酸与足量金属钠反应产生氢气的量不相同 |
3.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
(1)请完成以下实验设计表(表中不要留空格):
(2)编号①实验测得容器中压强随时间变化如图2.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式是O2+2H2O+4e-=4OH-.
(3)经过相当长的一段时间,图1锥形瓶中混合物表面生成了一层红棕色的铁锈,取少量铁锈于试管中,加入稀盐酸,取少量反应之后的溶液检验其中的Fe3+,检验Fe3+最灵敏的试剂是大家熟知的KSCN,可以检验痕量的Fe3+.还可用KI来检验:2Fe3++2I-?2Fe2++I2,有资料认为这可能是一个可逆反应.Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表.0.1mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水.

(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
(3)经过相当长的一段时间,图1锥形瓶中混合物表面生成了一层红棕色的铁锈,取少量铁锈于试管中,加入稀盐酸,取少量反应之后的溶液检验其中的Fe3+,检验Fe3+最灵敏的试剂是大家熟知的KSCN,可以检验痕量的Fe3+.还可用KI来检验:2Fe3++2I-?2Fe2++I2,有资料认为这可能是一个可逆反应.Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表.0.1mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水.
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量该FeCl3溶液和过量(填少量、过量)的KI溶液. | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至分液漏斗(填仪器)中,倒入一定量的CCl4,塞住活塞,充分振荡(萃取),静置. | 液体分层,上层接近无色,下层紫红色 |
| ③ | 打开活塞,先放出下层液体,再从分液漏斗的上口中倒出水层于试管中,加入KSCN溶液 | 出现血红色,则反应后的混合物中含Fe3+,进而证明这的确是一个可逆反应;反之则不含Fe3+,进而证明不是一个可逆反应 |

10.在有机化学中,需要加热的实验很多.下列不能用水浴加热的实验是( )
| A. | 苯的硝化反应 | B. | 银镜反应 | C. | 制酚醛树脂 | D. | 由乙醇制乙醚 |
20.现有三组混合液:①硝基苯和氢氧化钠溶液 ②苯和甲苯 ③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
7.气态反应 A(g)+3B(g)═2C(g)+2D(g),在四种不同条件下的反应速率最快的是( )
| A. | v(A)=0.15 mol/(L•s) | B. | v(B)=0.8 mol/(L•s) | C. | v(C)=0.4 mol/(L•s) | D. | v(D)=0.6 mol/(L•s) |
4.38.4毫克铜跟适量的浓硝酸反应,铜全部作用后共收集到气体33.6毫升(标准状况),反应消耗的HNO3的物质的量可能是( )
| A. | 1.0×10-3摩尔 | B. | 1.6×10-3摩尔 | C. | 2.2×10-3摩尔 | D. | 2.7×10-3摩尔 |
5.下列各组中的反应原理相同的是( )
| A. | 乙醇与浓硫酸共热140℃、170℃均能脱去水分子 | |
| B. | 甲苯、乙烯均能使酸性KMnO4溶液褪色 | |
| C. | 溴水中加入己烯或苯充分振荡,溴水层均褪色 | |
| D. | 1-溴丙烷分别与KOH水溶液、KOH乙醇溶液共热,均生成KBr |
 如图是某同学设计的放热反应的观察装置,其实验操作步骤如下:①按图所示将实验装置连接好,②在U形管内加入少量红墨水,打开T形管活塞,使U形管内两边的液面处于同一水平面,再关闭T形管活塞,③在盛有1g氧化钙的小试管里滴入2mL左右的蒸馏水,观察现象.
如图是某同学设计的放热反应的观察装置,其实验操作步骤如下:①按图所示将实验装置连接好,②在U形管内加入少量红墨水,打开T形管活塞,使U形管内两边的液面处于同一水平面,再关闭T形管活塞,③在盛有1g氧化钙的小试管里滴入2mL左右的蒸馏水,观察现象.