题目内容
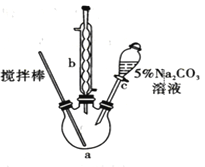
【题目】丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的装置如图所示:
制取的反应原理:CH2 =CHCOOH + HOCH3![]() CH2=CHCOOCH3 + H2O。
CH2=CHCOOCH3 + H2O。
可能用到的信息如下表:
沸点 | 溶解性 | 性质 | |
丙烯酸 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
丙烯酸甲酯 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
(一)制取丙烯酸甲酯
①取0.14mol丙烯酸、0.2mol的甲醇、少量的浓硫酸放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,加热。
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性。
③分液,取上层油状液体,再加无水Na2SO4后,蒸馏,收集馏分。
(二)检验丙烯酸甲酯的产率,设计如下实验:
①将收集的油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol·L-1的KOH溶液10.00 mL,加热使之完全水解。
②用酚酞作指示剂,向冷却后的溶液中滴加0.5 mol·L-1的盐酸,滴定到终点时共消耗盐酸20.00 mL。
回答下列问题:
(1)仪器b的名称是_________________。
(2) 浓硫酸的作用_________________。
(3) 搅拌棒的作用:___________ ; 5% Na2CO3溶液的作用:______________。
(4) 加无水Na2SO4的作用:_____________ ;蒸馏收集___________温度的馏分。
(5) 滴定终点的判断:_________________________________________________。
(6)计算本次酯化反应中丙烯酸的转化率为____________(计算结果保留到小数点后一位)。
【答案】 冷凝管(或球形冷凝管) 催化剂 混合均匀,加快反应速率_ 除去浓硫酸、丙烯酸等酸 干燥剂(除去有机层中的水) 80.5℃ 当最后一滴HCl溶液滴入锥形瓶时,溶液由粉红色变成无色,且30s内不变色 53.6%
【解析】本题考查有机物的实验室制备,实验原理是酸与醇的酯化反应,属于可逆反应,为了提高产物的产率及提搞反应物的转化率,实验中采取了搅拌、将挥发出的反应物及时冷却回流等措施。
(1)仪器b的名称是冷凝管
(2)浓硫酸做催化剂,起催化的作用。
(3)搅拌棒的作用是:使反应物均匀混合,加快反应速率;碳酸钠可与硫酸、丙烯酸发生化学反应而除去,其作用是:除去浓硫酸、丙烯酸等酸
(4)Na2SO4固体可以吸水生成结晶水化物从而除去有机层中的水,Na2SO4的作用是:干燥剂(除去有机层中的水);丙烯酸甲酯的沸点为80.5℃,故应蒸馏收集80.5℃温度的馏分。
(5)丙烯酸甲酯在KOH的条件下发生彻底的水解反应,多余的KOH用HCl溶液中和滴定,用酚酞作指示剂,当滴入最后一滴盐酸时,溶液的颜色由红色变为无色,且30s内不恢复。答案为:当最后一滴HCl溶液滴入锥形瓶时,溶液由粉红色变成无色,且30s内不变色 。
(6) 0.14mol丙烯酸、0.2mol的甲醇理论上可以生成0.14mol丙烯酸甲酯;实验中:每份丙烯酸甲酯水解消耗的KOH的物质的量为(2.5×10-0.5×20)×10-3mol=0.015mol,丙烯酸甲酯与KOH按照物质的量之比1:1反应,所以总的丙烯酸甲酯的物质的量为0.015×5mol=0.075mol,所以产率为:0.075/0.14×100%=53.6%

【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A. 反应达到平衡时,X的转化率为50%
B. 反应可表示为X+3Y![]() 2Z
2Z
C. 增大压强使平衡向生成Z的方向移动,平衡常数增大
D. 升高温度平衡常数增大,则此反应为吸热反应
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为___。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中 为:___,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:___,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)Bodensteins研究了下列反应:2HI(g)H2(g)+I2(g) ΔH=+11kJ·mol-1,
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为___。若起始时n(HI)=100mol,则过程中需吸收的能量为___kJ。
②上述反应中,正反应速率为v正=k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为___(以K和k正表示)。
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为___(填字母)

【题目】元素单质及其化合物有广泛用途,请回答下列问题:
(1)第三周期元素中,钠原子核外有_______种能量不同的电子;氯原子的最外层电子排布式为______________;由这两种元素组成的化合物的电子式为__________。
(2)下列气体能用浓硫酸干燥的是________。
A.NH3 B.HI C.SO2 D.CO2
(3)请用一个实验事实说明钠与镁的金属性强弱________________________________。
(4)KClO3可用于实验室制O2,若不加催化剂,400 ℃时可分解生成两种盐,化学方程式为:KClO3 ![]() KCl+KClO4 (未配平),则氧化产物与还原产物的物质的量之比为_________。
KCl+KClO4 (未配平),则氧化产物与还原产物的物质的量之比为_________。
(5)已知:
化合物 | MgO | MgCl2 |
类型 | 离子化合物 | 离子化合物 |
熔点/℃ | 2800 | 714 |
工业上电解MgCl2制单质镁,而不电解MgO的原因是________________________________。
